题目内容
下列叙述中不正确的是( )
| A、2.0 g重水(D2O)中含有的质子数和中子数都为1.0 NA |
| B、pH>7的溶液中:Na+、K+、CO32-、ClO一、S2-不能大量共存 |
| C、向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动 |
| D、酒精溶于水时没有破坏化学键 |
考点:离子共存问题,质量数与质子数、中子数之间的相互关系,化学键,水的电离
专题:离子反应专题
分析:A.重水的摩尔质量为20g/mol,重水分子中含有的质子数和中子数都是10;
B.pH>7的溶液为碱性溶液,次氯酸根离子能够氧化硫离子;
C.水的离子积只受温度影响,加入盐酸后温度不变,则水的离子积不变;
D.酒精溶于水没有发生电离,则没有破坏化学键.
B.pH>7的溶液为碱性溶液,次氯酸根离子能够氧化硫离子;
C.水的离子积只受温度影响,加入盐酸后温度不变,则水的离子积不变;
D.酒精溶于水没有发生电离,则没有破坏化学键.
解答:
解:A.2.0g重水的物质的量为0.1mol,0.1mol重水分子中含有1mol质子、1mol中子,含有的质子数和中子数都为1.0NA,故A正确;
B.ClO-、S2-之间发生氧化还原反应,在溶液中不能大量共存,故B正确;
C.降低温度,水的离子积减小,而加入盐酸,不影响水的离子积,故C错误;
D.酒精不是电解质,加入水中没有发生电离,则没有破坏化学键,故D正确;
故选C.
B.ClO-、S2-之间发生氧化还原反应,在溶液中不能大量共存,故B正确;
C.降低温度,水的离子积减小,而加入盐酸,不影响水的离子积,故C错误;
D.酒精不是电解质,加入水中没有发生电离,则没有破坏化学键,故D正确;
故选C.
点评:本题考查了离子共存的判断、水的离子积的影响、化学键等知识,题目难度中等,注意掌握离子共存的判断方法,明确水的离子积只受温度影响,温度不变则水的离子积不变.

练习册系列答案
相关题目
下列关于有机物的叙述正确的是( )
| A、石油的分馏和裂化均属于化学变化 |
| B、乙醇、乙酸能用碳酸钠溶液、紫色石蕊溶液、酸性高锰酸钾溶液等多种方法鉴别 |
| C、油脂、塑料、天然橡胶都是高分子化合物 |
| D、因为葡萄糖在糖类结构中最简单,因此它是一种单糖 |
下列叙述正确的是( )
| A、甲苯、苯乙烯都能使酸性高锰酸钾溶液褪色,也都能与溴的四氯化碳溶液反应而褪色 |
| B、天然气和液化石油气的主要成分都是烃 |
| C、溴乙烷和乙醇在相同的反应条件下都可以生成乙烯 |
| D、石蜡是从石油中获取的油脂 |
常温下,水的离子积为Kw,下列说法正确的是( )
| A、在pH=11的溶液中,水电离出的c(OH-)一定等于10-3mol/L |
| B、将pH=1的酸和pH=13的碱溶液等体积混合后,溶液的pH一定等于7 |
| C、一元酸HA与一元碱BOH混合后,溶液中c(A-)=c(B+),则溶液呈中性 |
| D、若强酸、强碱中和后溶液的pH=7,则中和之前酸、碱的pH之和一定等于14 |
下列关于有机化合物的叙述正确的是( )
| A、用NaOH溶液可以除去乙酸乙酯中的乙酸 |
| B、乙烯和苯都能与溴水反应而使溴水褪色 |
| C、用新制的银氨溶液可区分甲酸甲酯和乙醛 |
| D、脂肪、糖类和蛋白质都是人体重要的营养物质 |
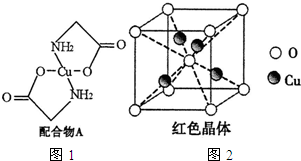 已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A.其结构如图1:
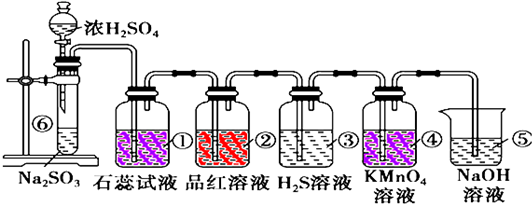
已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A.其结构如图1: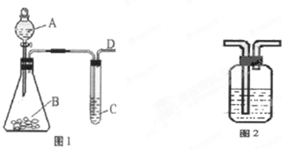 某同学用如图1所示的装置来探究SO2的性质及有关实验.
某同学用如图1所示的装置来探究SO2的性质及有关实验.