题目内容
下列事实,不能用勒夏特列原理解释的是( )
| A、SO2催化氧化成SO3的反应,往往加入过量的空气 |
| B、合成氨工业中不断从反应混合物中液化分离出氨气 |
| C、实验室中常用排饱和食盐水的方法收集Cl2 |
| D、二氧化氮与四氧化氮的平衡体系,加压缩小体积后颜色加深 |
考点:化学平衡移动原理
专题:化学平衡专题
分析:勒夏特列原理是:如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动.勒夏特列原理适用的对象应存在可逆过程,若与可逆过程无关,与平衡移动无关,则不能用勒夏特列原理解释.
解答:
解:A、存在平衡2SO2+O2(g)?2SO3(g),加入过量的空气,平衡向正反应方向移动,提高二氧化硫的转化率,能用勒夏特利原理解释,故A错误;
B、存在平衡N2(g)+3H2(g)?2NH3(g),不断从反应混合物中液化分离出氨气,平衡向正反应方向移动,能用勒夏特利原理解释,故B错误;
C、氯气和水反应生成盐酸和次氯酸,该反应存在溶解平衡,饱和食盐水中含有氯化钠电离出的氯离子,饱和食盐水抑制了氯气的溶解,所以实验室可用排饱和食盐水的方法收集氯气,能用勒夏特利原理解释,故C错误;
D、该反应是一个气体体积减小的可逆反应,加压缩小体积时容器中二氧化氮的浓度增大而使气体颜色加深,而不是四氧化二氮转化为二氧化氮而使气体颜色加深,不能用勒夏特列原理解释,故D正确.
故选D.
B、存在平衡N2(g)+3H2(g)?2NH3(g),不断从反应混合物中液化分离出氨气,平衡向正反应方向移动,能用勒夏特利原理解释,故B错误;
C、氯气和水反应生成盐酸和次氯酸,该反应存在溶解平衡,饱和食盐水中含有氯化钠电离出的氯离子,饱和食盐水抑制了氯气的溶解,所以实验室可用排饱和食盐水的方法收集氯气,能用勒夏特利原理解释,故C错误;
D、该反应是一个气体体积减小的可逆反应,加压缩小体积时容器中二氧化氮的浓度增大而使气体颜色加深,而不是四氧化二氮转化为二氧化氮而使气体颜色加深,不能用勒夏特列原理解释,故D正确.
故选D.
点评:本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆过程,且平衡发生移动.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
下列物质属于纯净物的是( )
| A、食盐水 | B、爆鸣气 |
| C、甲烷 | D、纯净的无污染的空气 |
将 17.9g 由 Al、Fe、Cu 组成的合金溶于足量的 NaOH 溶液中,产生气体 3.36L(标准状况).另取等质量的合金溶于过量的稀硝酸中,向反应后的溶液中加入过量的NaOH 溶液,得到沉淀的质量为 25.4g.若 HNO3的还原产物仅为 NO,则生成 NO的标准状况下的体积为( )
| A、2.24L |
| B、4.48L |
| C、6.72L |
| D、8.96L |
下列分子均属于极性分子且中心原子均为sp3杂化的是( )
| A、NH3、H2O |
| B、SO2、SCl2 |
| C、PCl3、SO3 |
| D、CH4、C60 |
NA代表阿伏加德罗常数,下列说法不正确的是( )
| A、一定量的Fe与含1mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA |
| B、1L 0.5mol/L Na2CO3溶液中含有的CO32-数目为0.5NA |
| C、标准状况下,2.24L Cl2与足量的Mg充分反应,转移的电子数目为0.2NA |
| D、0.1mol CH4所含的电子数为NA |
下列化学用语正确的是( )
A、中子数为8的N原子:
| ||
B、硫离子的结构示意图: | ||
| C、H2O2的结构式:H-O-O-H | ||
| D、石英的化学式:Na2SiO3 |
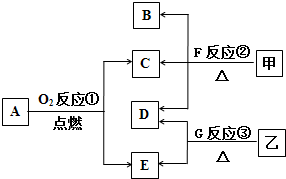 物质A~G及甲、乙有如图转化关系.
物质A~G及甲、乙有如图转化关系.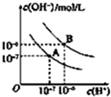 (1)写出下列物质溶于水的电离方程式
(1)写出下列物质溶于水的电离方程式