题目内容
用铁片与稀硫酸反应制取氢气时,下列措施能使氢气生成速率加快的是( )
| A、滴加少量硫酸铜溶液 |
| B、增多铁片的用量 |
| C、改用98%的浓硫酸 |
| D、加入少量的CH3COONa固体 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:影响铁与稀硫酸反应的因素有浓度、温度、固体表面积大小以及原电池反应等,一般来说,增大浓度、升高温度、增大固体表面积或形成原电池反应都可增大反应速率.
解答:
解:A.加少量硫酸铜,锌置换出铜,形成原电池反应,反应速率增大,故A正确;
B.铁为固体,增加铁的量,浓度不变,反应速率不变,故B错误;
C.改用98%的浓硫酸,不生成氢气,则生成氢气的反应速率减小,故C错误;
D.加入少量的CH3COONa固体,生成醋酸,氢离子浓度减小,反应速率减小,故D错误.
故选A.
B.铁为固体,增加铁的量,浓度不变,反应速率不变,故B错误;
C.改用98%的浓硫酸,不生成氢气,则生成氢气的反应速率减小,故C错误;
D.加入少量的CH3COONa固体,生成醋酸,氢离子浓度减小,反应速率减小,故D错误.
故选A.
点评:本题考查化学反应速率的影响,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意把握影响化学反应速率的影响和影响原因,难度不大,注意相关基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
从海水中提取镁的工业流程如图所示,下列说法正确的是( )

| A、在实验室进行②的操作需用到坩埚、坩埚钳、玻璃棒、酒精灯 |
| B、步骤⑥电解MgCl2时,阴极产生H2 |
| C、步骤⑤应将晶体置于HCl气体氛围中脱水 |
| D、上述工艺流程中的反应未涉及氧化还原反应 |
可逆反应aA(g)+bB(g)?cC(g)+dD(g)△H=Q,同时符合下列两图中各曲线的规律的是( )

| A、a+b>c+d T1<T2 Q<0 |
| B、a+b>c+d T1>T2 Q>0 |
| C、a+b<c+d T1>T2 Q>0 |
| D、a+b>c+d T1>T2 Q<0 |
把足量的铁粉投入到稀盐酸和氯化铜的混合溶液中,充分反应后,残余固体的质量与原来加入的铁粉质量相等,则原溶液中H+和Cl-的物质的量之比为( )
| A、1:4 | B、1:7 |
| C、1:8 | D、2:5 |
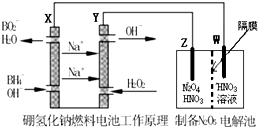 N2O5是一种新型绿色硝化剂,一种制备方法是用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5.工作原理如图:(隔膜不允许水分子通过,H+可以通过)下列说法正确的是( )
N2O5是一种新型绿色硝化剂,一种制备方法是用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5.工作原理如图:(隔膜不允许水分子通过,H+可以通过)下列说法正确的是( )| A、Y是负极,电极反应式:H2O2+2e-=2OH- |
| B、Z是阳极,电极反应式为:N2O4+2HNO3-2e-=2N2O5+2H+ |
| C、电流从X流出经导线流入W极 |
| D、制备10.8gN2O5至少需要消耗硼氢化钠0.87g |
已知反应:①101kPa时,2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
又知由H2和O2两种气体反应生成1mol液态水比生成1mol气态水多放出44kJ热量.下列结论中正确的是( )
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
又知由H2和O2两种气体反应生成1mol液态水比生成1mol气态水多放出44kJ热量.下列结论中正确的是( )
| A、H2的燃烧热为285.8 kJ/mol | ||
B、H2和O2反应生成液态水时的热化学方程式为H2(g)+
| ||
| C、稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ | ||
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
下列化学用语表示不正确的是( )
A、Na+的结构示意图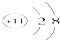 |
B、四氯化碳的电子式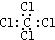 |
| C、二氧化碳的结构式为O=C=O |
| D、乙烯的实验式为 CH2 |