题目内容
某温度下,反应N2O4(g)?2NO2(g),△H>0,在体积可变的密闭容器中达到平衡.下列说法正确的是( )
| A、保持温度和体积不变,加入少许N2O4,再达到平衡时,颜色变深,N2O4转化率减小 |
| B、保持温度和体积不变,加入少许NO2,将使正反应速率减小 |
| C、保持温度不变,增大压强时,将使正反应速率增大,逆反应速率减小 |
| D、保持体积不变,升高温度,再达平衡时颜色变浅 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、保持温度和体积不变,加入少许N2O4,所到达平衡状态,等效为在原平衡的基础上增大压强;
B、保持温度和体积不变,加入少许NO2,达到平衡状态,等效为原平衡状态的基础上增大压强;
C、压强增大正逆反应速率都增大;
D、反应是吸热反应,升温平衡正向进行,达到平衡状态气体颜色加深;
B、保持温度和体积不变,加入少许NO2,达到平衡状态,等效为原平衡状态的基础上增大压强;
C、压强增大正逆反应速率都增大;
D、反应是吸热反应,升温平衡正向进行,达到平衡状态气体颜色加深;
解答:
解:A、保持温度和体积不变,加入少许N2O4,所到达平衡状态,等效为在原平衡的基础上增大压强,平衡状态浓度增大,气体颜色加深,平衡逆向进行,N2O4转化率减小,故A正确;
B、保持温度和体积不变,加入少许NO2,达到平衡状态,等效为原平衡状态的基础上增大压强,反应速率增大,正逆反应速率都增大,故B错误;
C、保持温度不变,压强增大正逆反应速率都增大,故C错误;
D、保持体积不变,反应是吸热反应,升温平衡正向进行,达到平衡状态气体颜色加深,故D错误;
故选A.
B、保持温度和体积不变,加入少许NO2,达到平衡状态,等效为原平衡状态的基础上增大压强,反应速率增大,正逆反应速率都增大,故B错误;
C、保持温度不变,压强增大正逆反应速率都增大,故C错误;
D、保持体积不变,反应是吸热反应,升温平衡正向进行,达到平衡状态气体颜色加深,故D错误;
故选A.
点评:本题考查化学平衡移动的影响因素,难度中等,结合理解平衡移动原理,结合反应特征和平衡移动方向分析.

练习册系列答案
相关题目
下列物质分离和提纯方法属于化学分离提纯法的是( )
| A、分离沙子和食盐水溶液 |
| B、从氯化钠和硝酸钾的混合物中提纯硝酸钾 |
| C、分离溶于水中的氯化钠 |
| D、将O2和CO2混合气体通过NaOH溶液除去CO2气体 |
2004年,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质,已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧,下列有关硫化羰的说法正确的是( )
| A、1 mol硫化羰在氧气中完全燃烧时转移6mol电子 |
| B、硫化羰可用作灭火剂 |
| C、CO2和COS结构相似都是非极性分子 |
| D、硫化羰熔点可能较高 |
同一周期三种非金属元素X、Y、Z,其最高价氧化物的水化物的酸性由强到弱的顺序是:HXO4>H2YO4>H3ZO4.下列说法正确的是( )
| A、元素的非金属性:X<Y<Z |
| B、气态氢化物的稳定性:HX>H2Y>ZH3 |
| C、阴离子的还原性:X->Y2->Z3- |
| D、X、Y、Z依次位于ⅤA族、ⅥA族、ⅦA族 |
HBr分子的电子式为( )
A、 |
| B、H+Br- |
C、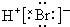 |
| D、H-Br |
下列根据实验现象所得出的结论中,一定正确的是( )
| A、无色溶液使红色石蕊试纸变蓝,结论:溶液显碱性 |
| B、无色溶液焰色反应呈黄色,结论:试液是钠盐溶液 |
| C、无色溶液加入Na2CO3溶液产生白色沉淀,结论:溶液中含Ca(OH)2 |
| D、无色溶液加入氢氧化钠溶液,加热产生的气体使红色石蕊试纸变蓝,结论:溶液中含NH3 |
某实验室用下列溶质配制一种混合溶液,已知溶液中存在c(K+)=c(Cl-)=0.5c(Na+)=c(SO42-),则其溶质可能是( )
| A、KCl,K2SO4 NaCl |
| B、KCl,Na2SO4,NaCl |
| C、NaCl,Na2SO4,K2SO4 |
| D、KCl,K2SO4,Na2SO4 |
在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A、K+、MnO4-、Na+、Cl- |
| B、Na+、K+、HCO3-、SO42- |
| C、K+、Na+、NO3-、CO32- |
| D、Fe3+、Na+、Cl-、SO42- |
4g某物质含有3.01×1022个分子,该物质的相对分子质量约为( )
| A、48 | B、16 | C、64 | D、80 |