题目内容
14.设NA为阿伏伽德罗常数值,下列叙述不正确的是( )| A. | 淀粉可用于酿酒 | |
| B. | 13g苯中含C-H键的数目是NA | |
| C. | C4H10O的醇有5种 | |
| D. | 标准状况下,11.2L甲烷和乙烯的混合物含氢原子数是2NA |
分析 A、淀粉水解为葡萄糖,葡萄糖在酒化酶的作用下生成酒精;
B、求出苯的物质的量,然后根据苯中含6条C-H键来分析;
C、丁基有4种;
D、求出混合气体的物质的量,然后根据甲烷和乙烯中均含4个H原子来分析.
解答 解:A、淀粉在稀硫酸做催化剂的条件下水解为葡萄糖,葡萄糖在酒化酶的作用下生成酒精,故淀粉可用于酿酒,故A正确;
B、13g苯的物质的量为$\frac{1}{6}$mol,而苯中含6条C-H键,故$\frac{1}{6}$mol苯中含C-H键个数为NA个,故B正确;
C、丁基有4种,故C4H10O的醇有4种,故C错误;
D、标况下11.2L混合气体的物质的量为0.5mol,而甲烷和乙烯中均含4个H原子,故0.5mol混合物中含2NA个H原子,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
3.欲证明一瓶无色液体是纯水,可靠的实验方法是( )
| A. | 1.01×105Pa时沸点为100℃ | B. | 测得其pH=7 | ||
| C. | 遇钠生成氢气 | D. | 电解时得到H2与O2的体积比为2:1 |
5.建设“碧水蓝天”的生态城市,下列措施中不合理的是( )
| A. | 大力实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染 | |
| B. | 积极推广太阳能、风能等新能源的使用,减少化石燃料的使用 | |
| C. | 加强城市生活污水脱氮除磷处理,遏制水体富营养化 | |
| D. | 加高烟囱,减少烟尘对周围环境的影响 |
2.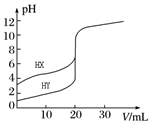 常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )
 常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL 0.10mol•L-1 的HX和HY溶液,滴定曲线如图所示.下列说法正确的是( )| A. | pH=7时,滴定HX消耗NaOH溶液体积等于20.00 mL | |
| B. | 将上述HX、HY溶液各加水稀释10倍,稀释后溶液的pH:pH(HY)>pH (HX) | |
| C. | 当NaOH溶液体积为20.00 mL时,HX溶液中离子浓度:c(Na+)>c(X-)>c(H+)>c(OH-) | |
| D. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,c(H+)+c(HX)=c(OH-) |
19.下列物质放在空气中变质,且变质过程与空气中的O2、CO2、水蒸气都有关的是( )
| A. | 过氧化钠 | B. | 金属钠 | C. | 硫酸亚铁晶体 | D. | 亚硫酸钠 |
6.有机物甲、乙的键线式结构如图所示.下列说法不正确的是( )
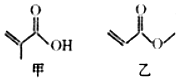
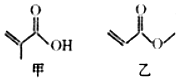
| A. | 甲和乙互为同分异构体 | |
| B. | 甲和乙都能发生取代反应 | |
| C. | 甲和乙中都有3种不同化学环境的氢 | |
| D. | 1mol甲和1mol乙都能与2molH2发生加成反应 |
3.化学与生产、生活密切联系.下列说法正确的是( )
| A. | 食品包装中使用生石灰或硅胶可吸收水分使食品保持干燥 | |
| B. | 将化工厂排放废气的烟囱加高可减少烟尘对环境的污染 | |
| C. | 将家用84消毒液与洁厕灵混合使用可提高去污效果 | |
| D. | 向海水中加明矾可使海水淡化 |
4.下列变化不需要破坏化学健的是( )
| A. | 加热氯化铵固体 | B. | 干冰气化 | C. | 石油裂化 | D. | 氯化氢溶于水 |

 ;
; ;
; .
.