题目内容
下列离子方程式正确的是( )
| A、碳酸氢钠水解:HCO3-+H2O?H3O++CO32- |
| B、醋酸铵溶于水:CH3COONH4+H2O?CH3COOH+NH3?H2O |
| C、硫酸氢钠溶液中滴入氢氧化钡溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| D、硫酸钙悬浊液中加入碳酸钠:CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq) |
考点:离子方程式的书写
专题:离子反应专题
分析:A、碳酸氢钠水解是结合水中的氢离子生成碳酸,这是电离方程式;
B、醋酸铵是强电解质,应写成离子的形式;
C、硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7,说明氢离子浓度与氢氧根离子浓度相等,都为1mol,同时溶液中1mol的硫酸根离子和0.5mol钡离子,硫酸根离子过量;
D、悬浊液作反应物应写成化学式的形式.
B、醋酸铵是强电解质,应写成离子的形式;
C、硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7,说明氢离子浓度与氢氧根离子浓度相等,都为1mol,同时溶液中1mol的硫酸根离子和0.5mol钡离子,硫酸根离子过量;
D、悬浊液作反应物应写成化学式的形式.
解答:
解:A、碳酸氢钠水解是结合水中的氢离子生成碳酸,这是电离方程式,正确的离子方程式为:HCO3-+H2O?OH-+H2CO3,故A错误;
B、醋酸铵是强电解质,应写成离子的形式,溶于水过程中涉及的离子反应为:CH3COO-+NH4++H2O?CH3COOH+NH3?H2O,故B错误;
C、硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7,说明氢离子浓度与氢氧根离子浓度相等,都为1mol,同时溶液中1mol的硫酸根离子和0.5mol钡离子,硫酸根离子过量,正确的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D、悬浊液应写成化学式的形式,正确的离子方程式为CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq),故D正确;
故选D.
B、醋酸铵是强电解质,应写成离子的形式,溶于水过程中涉及的离子反应为:CH3COO-+NH4++H2O?CH3COOH+NH3?H2O,故B错误;
C、硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7,说明氢离子浓度与氢氧根离子浓度相等,都为1mol,同时溶液中1mol的硫酸根离子和0.5mol钡离子,硫酸根离子过量,正确的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D、悬浊液应写成化学式的形式,正确的离子方程式为CaSO4(s)+CO32-(aq)?CaCO3(s)+SO42-(aq),故D正确;
故选D.
点评:本题考查离子方程式的书写,题目难度较大,注意从化学式、离子符号、过量问题以及是否符合反应实际的角度分析.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
对于Cl2+SO2+2H2O═H2SO4+2HCl反应,下列说法正确的是( )
①Cl2是氧化剂 ②SO2被氧化 ③Cl2被氧化 ④Cl2发生还原反应 ⑤SO2具有还原性 ⑥Cl2具有氧化性.
①Cl2是氧化剂 ②SO2被氧化 ③Cl2被氧化 ④Cl2发生还原反应 ⑤SO2具有还原性 ⑥Cl2具有氧化性.
| A、只有①②⑥ |
| B、只有②③④ |
| C、只有②④⑤⑥ |
| D、只有①②④⑤⑥ |
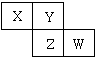 如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的
如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,若W原子最外电子层电子数是其内层电子数的| 7 |
| 10 |
| A、X元素的氢化物水溶液呈碱性 |
| B、气态氢化物的稳定性:Y>Z |
| C、最高氧化物对应水化物的酸性:W>Z |
| D、阴离子半径从大到小排列的顺序:Y>Z>W |
 CCTV-1《焦点访谈》栏目中曾报道“铊中毒事件”,铊再次成为公众关注的焦点.铊的相关信息如图,其中“6s26p1”表示铊原子有6个电子层,最外层有3个电子.下列有关卡片信息解读不正确的是( )
CCTV-1《焦点访谈》栏目中曾报道“铊中毒事件”,铊再次成为公众关注的焦点.铊的相关信息如图,其中“6s26p1”表示铊原子有6个电子层,最外层有3个电子.下列有关卡片信息解读不正确的是( )| A、铊的元素符号为Tl |
| B、铊原子的中子数为204 |
| C、铊位于第六周期ⅢA族 |
| D、铊的金属性比铝的金属性强 |
可逆反应N2(g)+3H2(g)?2NH3(g)在一定条件下于10L的密闭容器中发生,若开始时加入2molN2、2molH2、0mol NH3,反应达到平衡时NH3的浓度不可能达到的值是( )
| A、0.1mol/L |
| B、0.02mol/L |
| C、0.05mol/L |
| D、0.15mol/L |
下列说法中,正确的是( )
| A、能发生银镜反应的化合物一定是醛 |
| B、甲醛、乙酸、甲酸甲酯具有相同的最简式 |
C、C2H5OH和 具有相同的官能团,具有相同的化学性质 具有相同的官能团,具有相同的化学性质 |
| D、分子内有苯环和羟基的化合物一定是酚类 |
不属于氧化还原反应的是( )
A、2Al+Fe2O3
| ||||
B、2Mg+CO2
| ||||
C、N2+3H2
| ||||
| D、CaO+H2O═Ca(OH)2 |
下列实验操作不正确的是( )
| A、NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体时即停止加热 |
| B、除去Fe(OH)3胶体中混有的Cl-离子,可用渗析的方法 |
| C、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| D、用四氯化碳萃取碘时,碘的四氯化碳溶液从分液漏斗上口倒出 |
不能作为比较元素原子得失电子能力相对强弱的依据是( )
| A、元素气态氢化物的稳定性 |
| B、元素单质熔、沸点高低 |
| C、金属间发生的置换 |
| D、非金属阴离子的还原性强弱 |