题目内容
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A、加入过氧化钠后的溶液中:Na+、K+、Cl-、SO32- |
| B、含大量Fe3+的溶液中:Mg2+、Cl-、SO42-、NO3- |
| C、与Al反应放出H2的溶液中:NH4+、Na+、SO42-、F- |
| D、无色透明溶液中:Al3+、Ca2+、I-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.过氧化钠具有氧化性,与SO32-发生氧化还原反应;
B.该组离子之间不反应;
C.与Al反应放出H2的溶液,为非氧化性酸或强碱溶液;
D.离子之间相互促进水解.
B.该组离子之间不反应;
C.与Al反应放出H2的溶液,为非氧化性酸或强碱溶液;
D.离子之间相互促进水解.
解答:
解:A.过氧化钠具有氧化性,与SO32-发生氧化还原反应,不能共存,故A错误;
B.该组离子之间不反应,可大量共存,故B正确;
C.与Al反应放出H2的溶液,为非氧化性酸或强碱溶液,酸溶液中不能存在F-,碱溶液中不能存在NH4+,故C错误;
D.Al3+、HCO3-离子之间相互促进水解,不能大量共存,故D错误;
故选B.
B.该组离子之间不反应,可大量共存,故B正确;
C.与Al反应放出H2的溶液,为非氧化性酸或强碱溶液,酸溶液中不能存在F-,碱溶液中不能存在NH4+,故C错误;
D.Al3+、HCO3-离子之间相互促进水解,不能大量共存,故D错误;
故选B.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子的反应为解答的关键,侧重氧化还原反应、水解反应、复分解反应的离子共存考查,综合性较强,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
下列物质间的转化可由一步反应完成的是( )
| A、SiO2→H2SiO3 |
| B、Cu(OH)2→Fe(OH)2 |
| C、CaCO3→Na2CO3 |
| D、Cu→Cu(NO3)2 |
下列从海水中提取镁的工艺流程中,你认为最合理的是( )
A、海水
| ||||||
B、海水
| ||||||
C、海水
| ||||||
D、海水
|
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
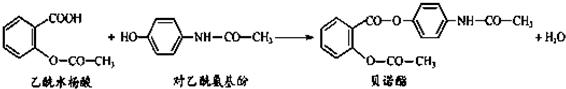
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A、贝诺酯分子中有三种含氧官能团 |
| B、对乙酰氨基酚核磁共振氢谱中共有四个峰 |
| C、乙酰水杨酸和对乙酰氨基酚均能与Na2CO3 溶液反应 |
| D、贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
关于钠的叙述中,正确的是( )
| A、钠是银白色金属,硬度很大 |
| B、金属钠在空气中燃烧,生成氧化钠 |
| C、金属钠的熔点很高 |
| D、加热时,金属钠剧烈燃烧,产生黄色火焰,生成过氧化钠 |
常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A、无色透明的溶液中:MnO4-、SO42-、K+、Fe2+ |
| B、c(OH-)/c(H+)=1012的水溶液中:K+、ClO-、S2-、Cl- |
| C、水电离出的c(H+)=10-12mol/L中:K+、AlO2-、CH3COO-、CO32- |
| D、能使加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- |
下列物质中所含分子数最多的是( )
| A、4℃时2.7mL 水 |
| B、2.24L一氧化碳(标准状况下) |
| C、6.02×1022个氯化氢分子 |
| D、4.9g 磷酸 |
下列说法中正确的是( )
| A、胶体带电荷,而溶液呈电中性 |
| B、胶体区别与其他分散系的本质特征是分散质粒子的大小 |
| C、某元素从化合态变为游离态时,该元素一定被还原 |
| D、醋酸、纯碱、石灰石、氨水分别属于酸、碱、盐和电解质 |
