题目内容
4.下列说法正确的是( )| A. | 制氢弹用到的D、T互为同位素 | |
| B. | 苛性钠溶液可用于治疗胃酸过多 | |
| C. | 硅胶可防止月饼等食品氧化变质 | |
| D. | 向海水中加入净水剂明矾可以使海水淡化 |
分析 A.质子数相同,中子数不同的同类元素的不同核素互为同位素;
B.苛性钠为氢氧化钠,具有较强的腐蚀性;
C.硅胶具有吸水性,不具有还原性;
D.向海水中加入净水剂明矾只能除去悬浮物杂质.
解答 解:A.D、T质子数都是1,二者中子数分别为1,2,所以二者互为同位素,故A正确;
B.苛性钠为氢氧化钠,具有较强的腐蚀性,不能用于治疗胃酸过多,故B错误;
C.硅胶具有吸水性,不具有还原性,可以防止食品受潮变质,不能防止食品氧化变质,故C错误;
D.向海水中加入净水剂明矾只能除去悬浮物杂质,不能减少盐的含量,不能使海水淡化,故D错误;
故选:A.
点评 本题考查了同位素判断、生活中常见药物、生活中常见的材料和食品添加剂、海水淡化,与生产生活接触密贴,明确相关物质的性质是解题关键,注意相关知识的积累.

练习册系列答案
相关题目
15.乙醇、正戊烷、苯是常见有机物,下列说法正确的是( )
| A. | 苯和溴水共热生成溴苯 | |
| B. | 2,2-二甲基丙烷是正戊烷的同系物 | |
| C. | 乙醇、正戊烷、苯均可通过石油的分馏得到 | |
| D. | 乙醇、正戊烷、苯均能发生取代反应和氧化反应 |
12.氰化钾(KCN)足常用的分析试剂,露置空气中吸收H2O和CO2产生HCN.下列叙述不正确的是( )
| A. | 氰化钾中含有离子键和极性键 | |
| B. | 氰化钾中碳元素的化合价为+4价 | |
| C. | KCN与KMnO4溶液反应可能生成CO2和N2 | |
| D. | 相同条件下,KCN溶液的碱性强于CH3COOK溶液 |
19.设NA为阿伏加德罗常数的数值,下列有关叙述正确的是( )
| A. | 100g 98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 16g16O2和18O2的混合物中含有的质子数目为8NA | |
| C. | 电解精炼铜的过程中,若阳极减重64g,则电路中一定通过2NA个电子 | |
| D. | 取50ml14.0mol/L浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA |
9.下列实验能达到目的是( )
| A. | 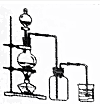 制备纯氯气 | B. | 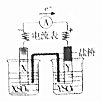 探究X、Y金属活泼性强弱 | ||
| C. | 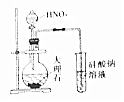 证明H2CO3酸性比H2SiO3强 | D. |  制备无水氯化铁 |
16.下列变化需要克服共价键的是( )
| A. | 干冰的升华 | B. | 硅的熔化 | C. | 氯化钾的溶解 | D. | 汞的气化 |
13.将后者逐渐滴入(或通入)前者至过量,有沉淀产生且最终消失的是( )
| A. | 氯化铝、氨水 | B. | 氢硫酸、氧气 | C. | 硫酸铝、氢氧化钠 | D. | 氯化亚铁、氯气 |
6.将下列气体通入酸性高锰酸钾溶液,能使酸性高锰酸钾溶液褪色的是( )
| A. | CH1 | B. | CO2 | C. | SO2 | D. | H2 |
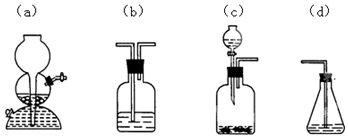
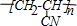 .
.