题目内容
如图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述不正确的是( )


| A、NaOH溶液的物质的量浓度为0.1mol/L |
| B、P点时反应恰好完全中和,溶液pH为7 |
| C、曲线a是NaOH人滴定盐酸的滴定曲线 |
| D、P点时溶液中的离子浓度为c(Na+)=c(Cl-)=c(H+)=c(OH-) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A、根据曲线b可以看出氢氧化钠溶液的pH=13,然后求出NaOH的物质的量浓度;
B、P点氢氧化钠与氯化氢恰好反应生成氯化钠,溶液中性中性;
C、根据曲线a的pH的变化趋势来判断;
D、根据曲线P点时pH值来判断酸碱性及溶液中各离子浓度大小.
B、P点氢氧化钠与氯化氢恰好反应生成氯化钠,溶液中性中性;
C、根据曲线a的pH的变化趋势来判断;
D、根据曲线P点时pH值来判断酸碱性及溶液中各离子浓度大小.
解答:
解:A、根据曲线b可知NaOH溶液的pH=13,则氢氧化钠溶液的浓度为:(NaOH)=0.1mol/L,故A正确;
B、P点时氢氧化钠与盐酸恰好反应,溶液呈中性,溶液的pH=7,故B正确;
C、曲线a的pH是由小到大,说明是氢氧化钠溶液滴定盐酸溶液的曲线,故C正确;
D、根据曲线可以看出P点时pH=7,说明溶液呈中性,c(Na+)=c(Cl-)、c(H+)=c(OH-),溶液中氢离子和氢氧根离子浓度很小则:c(Na+)=c(Cl-)>c(H+)=c(OH-),故D错误;
故选D.
B、P点时氢氧化钠与盐酸恰好反应,溶液呈中性,溶液的pH=7,故B正确;
C、曲线a的pH是由小到大,说明是氢氧化钠溶液滴定盐酸溶液的曲线,故C正确;
D、根据曲线可以看出P点时pH=7,说明溶液呈中性,c(Na+)=c(Cl-)、c(H+)=c(OH-),溶液中氢离子和氢氧根离子浓度很小则:c(Na+)=c(Cl-)>c(H+)=c(OH-),故D错误;
故选D.
点评:本题考查中和滴定、溶液中离子浓度大小比较,题目难度中等,试题借助于滴定曲线考查了中和滴定过程中PH的变化,注意掌握比较溶液中离子浓度大小的方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
如图是元素周期表短周期的一部分.其中F原子的电子层数为n,最外层电子数为2n+1,核内质子数为2n2-1.下列说法不正确的是( )
| A | B | C | |
| D | E | F |
| A、D的单质是常见的半导体材料 |
| B、B与E形成的化合物不只一种 |
| C、C与F的原子序数之差一定为8 |
| D、C属于卤族元素,对应的单质能与水反应生成两种酸 |
形形色色的硅酸盐存在于地球的每一个角落,在人类的生活和生产中扮演着重要的角色,下列说法不正确的是( )
| A、古代的陶瓷、砖瓦,现代的玻璃、水泥等,都是硅酸盐产品 |
| B、硅晶体的导电性介于导体和绝缘体之间,是一种重要的半导体材料 |
| C、硅酸、二氧化硅、硅酸钠及硅酸盐产品均属于电解质 |
| D、青花瓷胎体的原料为高岭土[Al2Si2O5(OH)4],若以氧化物形式科表示为:Al2O3?2SiO2?2H2O |
下列有关阿伏加德罗常数的叙述中,正确的( )
| A、30g甲醛中含有的共用电子对数为4NA |
| B、46 g NO2和N2O4的混合物中含有的原子数为3NA |
| C、5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA |
| D、将0.1 mol?L-1 FeCl3溶液制成胶体,该胶体中含有的胶粒数一定小于0.1NA |
苯在一定条件下可与浓HNO3发生如下反应 ,该反应属于( )
,该反应属于( )
 ,该反应属于( )
,该反应属于( )| A、加成反应 | B、酯化反应 |
| C、取代反应 | D、氧化反应 |
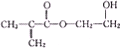 甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )
甲基丙烯酸烃乙酯是一种有机合成中重要的原料,其结构简式如图所示,下列有关说法错误的是( )| A、能发生加成反应 |
| B、能发生取代反应 |
| C、一定条件下,能与乙醇发生酯化反应 |
| D、既能是溴水褪色,又能使酸性高猛酸钾溶液褪色 |
NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、含0.1mol BaCl2的溶液中Cl-数为0.2NA |
| B、22g CO2所含有的分子数为0.5NA 已知M(CO2)=44g/mol |
| C、11.2L CO2所含有的分子数为0.5NA |
| D、常温下NA个N2分子电子数为14NA |
