��Ŀ����
����A��B��C��D��E��F����Ԫ�أ�Aԭ�Ӻ���ֻ��һ�����ӣ�B�����������Ǵ�����������2����CԪ�ص����������ӵ�3d�ܼ�Ϊ������� Eԭ�ӵ�M���N��ֱ��Dԭ�ӵ�M���N���5�����ӣ�Fԭ�ӵ�N��ֻ��һ�����ӣ���M��Ϊȫ������
��1��д��B�Ļ�̬ԭ�ӵļ۵��ӹ����ʾʽ
��2��C��Ԫ�ط��� �����̬ԭ�ӵĵ����Ų�ʽΪ
��3����E��C�ܷ�Ӧ�������ӻ�����CE3����D��ԭ�ӽṹʾ��ͼΪ ��A��B��ԭ�Ӹ�����Ϊ1��1��ɵ���Է�������Ϊ78�ķ�������E�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ
��4����Ԫ��F������������μ��백ˮ��������д���ù����漰��Ӧ�����ӷ���ʽ�� ��
��1��д��B�Ļ�̬ԭ�ӵļ۵��ӹ����ʾʽ
��2��C��Ԫ�ط���
��3����E��C�ܷ�Ӧ�������ӻ�����CE3����D��ԭ�ӽṹʾ��ͼΪ
��4����Ԫ��F������������μ��백ˮ��������д���ù����漰��Ӧ�����ӷ���ʽ��
���㣺λ�ýṹ���ʵ����ϵӦ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
������Aԭ�Ӻ���ֻ��һ�����ӣ���AΪ��Ԫ�أ�B�����������Ǵ�����������2����ԭ�Ӻ�������Ų�Ϊ1s22s22p2����BΪ̼Ԫ�أ�CԪ�ص����������ӵ�3d�ܼ�Ϊ���������Cԭ�ӵ����Ų�ʽΪ��1s22s22p63s23p63d64s2��Ϊ��Ԫ�أ�Eԭ�ӵ�M���N��ֱ��Dԭ�ӵ�M���N���5�����ӣ���Eԭ��3d������Dԭ��d���Ϊ3d5��N��Ϊ4s1��4s2��DΪCr��MnԪ�أ���EΪSe��BrԪ�أ�Fԭ�ӵ�N��ֻ��һ�����ӣ���M��Ϊȫ��������Fԭ�ӵĺ������=2+8+18+1=29����FΪCuԪ�أ��ݴ˽��
���
�⣺Aԭ�Ӻ���ֻ��һ�����ӣ���AΪ��Ԫ�أ�B�����������Ǵ�����������2����ԭ�Ӻ�������Ų�Ϊ1s22s22p2����BΪ̼Ԫ�أ�CԪ�ص����������ӵ�3d�ܼ�Ϊ���������Cԭ�ӵ����Ų�ʽΪ��1s22s22p63s23p63d64s2��Ϊ��Ԫ�أ�Eԭ�ӵ�M���N��ֱ��Dԭ�ӵ�M���N���5�����ӣ���Eԭ��3d������Dԭ��d���Ϊ3d5��N��Ϊ4s1��4s2��DΪCr��MnԪ�أ���EΪSe��BrԪ�أ�Fԭ�ӵ�N��ֻ��һ�����ӣ���M��Ϊȫ��������Fԭ�ӵĺ������=2+8+18+1=29����FΪCuԪ�أ�
��1��BΪ̼Ԫ�أ�CԪ�صĻ�̬�ļ۵��ӹ����ʾʽΪ��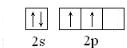 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��CΪ��Ԫ�أ������Ų�ʽΪ��1s22s22p63s23p63d64s2���ʴ�Ϊ��Fe��1s22s22p63s23p63d64s2��
��3����E��C�ܷ�Ӧ�������ӻ�����CE3��CΪ������E��-1�ۣ�ΪBrԪ�أ���DΪMnԪ�أ�25MnΪ25��Ԫ�أ�ԭ�Ӻ�����25�����ӣ�������25�����ӣ���ԭ��ṹʾ��ͼΪ�� ��H��C��ԭ�Ӹ�����Ϊ1��1��ɵ���Է�������Ϊ78�ķ�����ΪC6H6����Br2�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ��
��H��C��ԭ�Ӹ�����Ϊ1��1��ɵ���Է�������Ϊ78�ķ�����ΪC6H6����Br2�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ��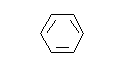 +Br2
+Br2
 +HBr
+HBr
�ʴ�Ϊ�� ��
�� +Br2
+Br2
 +HBr��
+HBr��
��4������ˮ��������ͭ��Һ�У����ȷ�����ӦCu2++2NH3?H2O=Cu��OH��2��+2NH4+��������ɫ�����������μӰ�ˮ����ӦΪCu��OH��2+4NH3��H2O=[Cu��NH3��4]2++4H2O+2OH-����ɫ�����ܽ⣬��Һ������ɫ���ʴ�Ϊ��Cu2++2NH3?H2O=Cu��OH��2��+2NH4+��Cu��OH��2+4NH3��H2O=[Cu��NH3��4]2++4H2O+2OH-��
��1��BΪ̼Ԫ�أ�CԪ�صĻ�̬�ļ۵��ӹ����ʾʽΪ��
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
����2��CΪ��Ԫ�أ������Ų�ʽΪ��1s22s22p63s23p63d64s2���ʴ�Ϊ��Fe��1s22s22p63s23p63d64s2��
��3����E��C�ܷ�Ӧ�������ӻ�����CE3��CΪ������E��-1�ۣ�ΪBrԪ�أ���DΪMnԪ�أ�25MnΪ25��Ԫ�أ�ԭ�Ӻ�����25�����ӣ�������25�����ӣ���ԭ��ṹʾ��ͼΪ��
 ��H��C��ԭ�Ӹ�����Ϊ1��1��ɵ���Է�������Ϊ78�ķ�����ΪC6H6����Br2�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ��
��H��C��ԭ�Ӹ�����Ϊ1��1��ɵ���Է�������Ϊ78�ķ�����ΪC6H6����Br2�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ�� +Br2
+Br2| FeBr3 |
 +HBr
+HBr�ʴ�Ϊ��
 ��
�� +Br2
+Br2| FeBr3 |
 +HBr��
+HBr����4������ˮ��������ͭ��Һ�У����ȷ�����ӦCu2++2NH3?H2O=Cu��OH��2��+2NH4+��������ɫ�����������μӰ�ˮ����ӦΪCu��OH��2+4NH3��H2O=[Cu��NH3��4]2++4H2O+2OH-����ɫ�����ܽ⣬��Һ������ɫ���ʴ�Ϊ��Cu2++2NH3?H2O=Cu��OH��2��+2NH4+��Cu��OH��2+4NH3��H2O=[Cu��NH3��4]2++4H2O+2OH-��
���������⿼��ṹ����λ�ù�ϵ�����ӽṹ����������Ų����ɵȣ��Ѷ��еȣ�ע�����֪ʶ���������գ���4��Ϊ�״��㣬ѧ��������������ͭ�����백ˮ��Ӧ�����İ���ͭ�����ӣ�

��ϰ��ϵ�д�
 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
�����Ŀ
ijǿ������Һ�п��ܴ���NO3-��I-��Cl-��Fe3+�е�һ�ֻ��֣������Һ�м�����ˮ���屻��ԭ���ɴ˿��ƶϸ���Һ�У�������
| A������NO3-�����ܺ�Fe3+ |
| B������NO3-��I-��Cl- |
| C����I-��������ȷ���Ƿ�Cl- |
| D��������NO3-��Fe3+ |
������NH4I�����ܱ������У���һ���¶��·������з�Ӧ��
��NH4I��s��?NH3��g��+HI��g������2HI��g��?H2��g��+I2��g��
�ﵽƽ��ʱ��c��H2��=0.5mol/L��c��HI��=6mol/L������¶��·�Ӧ�ٵ�ƽ�ⳣ��Ϊ��������
��NH4I��s��?NH3��g��+HI��g������2HI��g��?H2��g��+I2��g��
�ﵽƽ��ʱ��c��H2��=0.5mol/L��c��HI��=6mol/L������¶��·�Ӧ�ٵ�ƽ�ⳣ��Ϊ��������
| A��49 | B��16 | C��36 | D��42 |
���³�ѹ�£��ڵ�������ܱ������г������������ѹǿ��С���ǣ�������
| A��0.3mol HCl��0.3molNH3 |
| B��0.2mol H2��0.1mol O2 |
| C��0.2mol NH3��0.1mol O2 |
| D��0.2mol N2��0.05mol H2 |
ù���ᣨMycophenolic acid����һ��������Ի���������й�ù�����˵������ȷ���ǣ�������
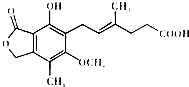

| A������ʽΪ��C17H20O6 |
| B���������ܷ����ӳɡ�ȡ�����Ӿ۵ȷ�Ӧ |
| C������������FeCl3��Һ������ɫ��Ӧ |
| D��һ�������£�1molù����������2molNaOH��Ӧ |