题目内容
8.设NA为阿伏加德罗常败的数值,下列说法错误的是( )| A. | 0.1 mol羟基 ( 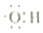 ) 中含有的电子数为0.7NA ) 中含有的电子数为0.7NA | |
| B. | 1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA | |
| C. | 由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COC-数目为NA | |
| D. | 14g乙烯与丙烯混合气体中的氢原子数为2NA |
分析 A、羟基中含9个电子;
B、钠反应后变为+1价;
C、由1mol CH3COONa和少量CH3COOH形成的中性溶液中满足电荷守恒:n(CH3COO-)+n(OH-)=n(Na+)+n(H+);
D、乙烯和丙烯的最简式均为CH2.
解答 解:A、羟基中含9个电子,故0.1mol-OH 中含0.9NA个电子,故A错误;
B、钠反应后变为+1价,故1mol钠反应后转移NA个电子,与产物无关,故B正确;
C、由1mol CH3COONa和少量CH3COOH形成的中性溶液中满足电荷守恒:n(CH3COO-)+n(OH-)=n(Na+)+n(H+),而由于是中性溶液,故n(OH-)=n(H+),则n(CH3COO-)=n(Na+)=1mol,即为NA个,故C正确;
D、乙烯和丙烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量为1mol,故含2NA个H原子,故D正确.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
19.能用H++OH-=H2O表示的是( )
| A. | NaHSO4+NaOH=Na2SO4+H2O | B. | CH3COOH+NaOH→CH3COONa+H2O | ||
| C. | H2SO4+Ba(OH)2→BaSO4↓+2H2O | D. | NH3•H2O+HCl→NH4Cl+H2O |
20.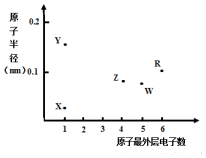 X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示.下列说法错误的是( )
X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示.下列说法错误的是( )
 X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示.下列说法错误的是( )
X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示.下列说法错误的是( )| A. | 简单离子半径:Y<W | |
| B. | 最高价氧化物对应水化物的酸性:Z<W | |
| C. | R为氧元素 | |
| D. | X与Z可以形成正四面体结构的分子 |
3.一些常见有机物的转化如图下列说法正确的是( )


| A. | 上述有机物中只有C6H12O6属于糖类物质 | |
| B. | 转化1可在人体内完成,该催化剂属于蛋白质 | |
| C. | 物质C和油脂类物质互为同系物 | |
| D. | 物质A和B都属于电解质 |
13.下列反应中氮元素既被氧化又被还原的是( )
| A. | 2NH3+3CuO $\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | 4HNO3(浓)$\frac{\underline{\;光照\;}}{或△}$4NO2↑+O2↑+2H2O | D. | N2+O2 $\frac{\underline{\;放电\;}}{\;}$ 2NO |
20.下列溶液中,与100ml 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A. | 100 ml 0.5 mol/L MgCl2 溶液 | B. | 200 ml 0.25 mol/L HCl溶液 | ||
| C. | 50 ml 1 mol/L NaCl溶液 | D. | 200 ml 0.25 mol/L CaCl2溶液 |
17.下列反应中,△S<0的是( )
| A. | H2(g)+Br2(g)?2HBr(g) | B. | 2N2O5(g)=4NO2(g)+O2(g) | ||
| C. | 2SO2(g)+O2?2SO3(g) | D. | CaCO3(s)=CaO(s)+CO2(g) |