��Ŀ����
���л�ѧ���������ȷ���ǣ� ��
A������ı�ȼ���ȡ�H=-890.3 kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(l) ��H=-890.3 kJ��mol-1
B����ϩ�ļ���ʽ��
C��һ�������£�ij�ܱ������г���2 mol SO2(g)��1 mol O2(g)���ﵽƽ��ų�Q
kJ��������������µ��Ȼ�ѧ����ʽΪ��2SO2(g)+O2(g) 2SO3(g
) ��H= -Q kJ��mol-1
2SO3(g
) ��H= -Q kJ��mol-1
D����ϩ�Ľṹ��ʽ��CH2CH2
���𰸡�
A
��������
���������A������ı�ȼ���ȡ�H=-890.3
kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(l)
��H=-890.3 kJ��mol-1����ȷ��B��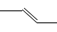 Ϊ2����ϩ�ļ���ʽ������C��2SO2+O2
Ϊ2����ϩ�ļ���ʽ������C��2SO2+O2 2SO3Ϊ���淴Ӧ�����淴Ӧ���ܽ��е��ף�һ�������£�ij�ܱ������г���2 mol SO2(g)��1 mol O2(g)���ﵽƽ��ų�Q
kJ��������������µ��Ȼ�ѧ����ʽ���ʱ��H�� -Q kJ��mol-1������D����ϩ�Ľṹ��ʽӦΪCH2=CH2������
2SO3Ϊ���淴Ӧ�����淴Ӧ���ܽ��е��ף�һ�������£�ij�ܱ������г���2 mol SO2(g)��1 mol O2(g)���ﵽƽ��ų�Q
kJ��������������µ��Ȼ�ѧ����ʽ���ʱ��H�� -Q kJ��mol-1������D����ϩ�Ľṹ��ʽӦΪCH2=CH2������
���㣺���黯ѧ���

��ϰ��ϵ�д�
�����Ŀ
���л�ѧ���������ȷ���ǣ�������
A����-�����ױ��Ľṹ��ʽ��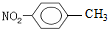 | B��NH4Cl�ĵ���ʽΪ��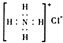 | C��H216O��D216O��Ϊͬ�������� | D����Ȳ�����ʽ��CH |
���л�ѧ���������ȷ���ǣ�������
A��S2-�Ľṹʾ��ͼ�� | B��NH3�Ľṹʽ��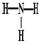 | C���Ȼ��Ƶĵ���ʽ��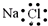 | D����ϩ�Ľṹ��ʽ��CH2CH2 |


