题目内容
2.用铜做电极,电解某浓度的AgNO3和Cu(NO3)2的混合溶液,一段时间后,阴极上析出1.6gCu时,不考虑溶液体积变化,则下列叙述中正确的是( )| A. | 电路中流过0.05mol电子 | B. | 溶液中c(Cu2+)降低 | ||
| C. | 电解质溶液质量减少 | D. | 阳极铜消耗了1.6g |
分析 电解AgNO3、Cu(NO3)2的混合液,首先在阴极上得电子的是Ag+,Ag++e-=Ag,其次是Cu2+,Cu2++2e-=Cu,在阳极上是铜失电子的过程,Ag++e-=Ag,根据电极反应:Cu2++2e-=Cu,此时转移电子是0.05mol,消耗铜离子是0.025mol,某浓度的AgNO3和Cu(NO3)2的混合溶液的浓度和体积不知,不能计算电子转移总数和阳极质量减小.
解答 解:电解AgNO3、Cu(NO3)2的混合液,首先在阴极上得电子的是Ag+,Ag++e-=Ag,其次是Cu2+,Cu2++2e-=Cu,在阳极上是铜失电子的过程,Ag++e-=Ag,根据电极反应:Cu2++2e-=Cu,此时转移电子是0.05mol,消耗铜离子是0.025mol,
A.某浓度的AgNO3和Cu(NO3)2的混合溶液的浓度和体积不知,不能计算电子转移总数,故A错误;
B.电解过程中电子守恒,阳极铜失电子发生氧化反应,同时阴极析出银和铜,溶液中铜离子浓度增大,故B错误;
C.电解过程中电子守恒,阳极铜失电子发生氧化反应,Cu-2e-=Cu2+,同时阴极析出银和铜,首先在阴极上得电子的是Ag+,Ag++e-=Ag,其次是Cu2+,Cu2++2e-=Cu,所以溶液质量减少,故C正确;
D.电子守恒分析可知阳极铜消耗质量大于1.6g,故D错误;
故选C.
点评 本题目是一道关于电解池的工作原理知识的计算题,注意阴极上阳离子的放电顺序以及阳极上的电极反应是关键,题目难度中等.

练习册系列答案
相关题目
12.现有CuO和Fe2O3的混合物a g,向其中加入1.0mol/L的硝酸溶液200mL,恰好完全反应.若将2a g该混合物用足量CO还原,充分反应后剩余固体的质量为( )
| A. | (2a-1.6)g | B. | 2(a-1.6)g | C. | (a-1.6)g | D. | (2a-3.2)g |
13.下列配合物的水溶液中加入硝酸银不能生成沉淀的是( )
| A. | [Co(NH3)4 Cl2]Cl | B. | [Co(NH3)3 Cl3] | C. | [Co(NH3)6]Cl3 | D. | [Cu(NH3)4]Cl2 |
10.下列叙述正确的是( )
| A. | 1 mol H2O的质量为18g•mol-1 | |
| B. | 标准状况下,1 mol任何物质体积均为22.4L | |
| C. | 3.01×1023个NH3分子的质量为8.5g | |
| D. | CH4的摩尔质量为16g |
17.糖类、油脂、蛋白质和维生素都是人类的基本营养物质.
①有些学生偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取维生素(选填“脂肪”、“维生素”或“蛋白质”)不足引起的.
②下表为某品牌燕麦片标签中的一部分.
燕麦片的营养成分中的蛋白质能水解成氨基酸;每克营养物质氧化时放出能量最多的是油脂;葡萄糖在人体内发生氧化反应的化学方程式:C6H12O6+6O2→6CO2+6H2O;人体必需的微量元素是锌.
①有些学生偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取维生素(选填“脂肪”、“维生素”或“蛋白质”)不足引起的.
②下表为某品牌燕麦片标签中的一部分.
| 每100g含有 营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 8.1mg |
14.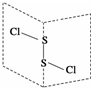 S2Cl2是广泛用于橡胶工业的硫化剂;其分子结构如图所示.常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中错误的是( )
S2Cl2是广泛用于橡胶工业的硫化剂;其分子结构如图所示.常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中错误的是( )
 S2Cl2是广泛用于橡胶工业的硫化剂;其分子结构如图所示.常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中错误的是( )
S2Cl2是广泛用于橡胶工业的硫化剂;其分子结构如图所示.常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中错误的是( )| A. | S2Cl2的电子式为 | |
| B. | S2Cl2为含有极性键和非极性键的非极性分子 | |
| C. | S2Br2与S2Cl2结构相似,熔、沸点:S2Br2>S2Cl2 | |
| D. | S2Cl2与H2O反应有SO2生成 |
11.关于乙烯的化学性质,说法错误的是( )
| A. | 可与H2发生加成反应 | B. | 能使溴水褪色 | ||
| C. | 不能发生聚合反应 | D. | 可与酸性高锰酸钾发生氧化反应 |