题目内容
7.下列说法正确的是( )| A. | 干冰升华时须吸收大量的热,这就是化学反应中的吸热现象 | |
| B. | 酒精常被用作酒精灯和内燃机的燃料,说明酒精燃烧是放热反应 | |
| C. | 木炭常温下不燃烧,加热才能燃烧,说明木炭燃烧是吸热反应 | |
| D. | 酸碱中和反应都放热,因此可以将其设计成原电池,将化学能转换成电能供人们使用 |
分析 A.干冰升华为物理变化;
B.酒精燃烧放出大量的热;
C.吸热反应、放热反应与是否加热无关;
D.原电池为自发进行的氧化还原反应.
解答 解:A.干冰升华为物理变化,不是化学变化,而吸热反应为化学变化,故A错误;
B.酒精燃烧放出大量的热,可用作燃料等,故B正确;
C.是否加热为诱发反应的条件,需要加热的不一定为吸热反应,如铝热反应等,木炭的燃烧必须达到着火点,故C错误;
D.原电池为自发进行的氧化还原反应,中和反应没有电子的转移,不能形成原电池反应,故D错误.
故选B.
点评 本题综合考查化学反应与能量变化,为高频考点,侧重考查学生的分析能力,注意把握能量转化的形式以及放热反应、吸热反应的区别,把握原电池的工作原理,难度不大.

练习册系列答案
相关题目
2.下列物质中,有非极性键的是( )
| A. | 氮气 | B. | 氯化镁 | C. | 水 | D. | 甲烷 |
18.下列说法正确的( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 离子化合物中只能含离子键 | |
| D. | 只有非金属原子间才能形成共价键 |
15.下列离子方程式正确的是( )
| A. | Cl2与NaOH溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | F2与NaOH溶液反应:F2+4OH-═2F-+O2+2H2O | |
| C. | AgNO3溶液中加入少量氨水:Ag++2NH3•H2O═Ag(NH3)2++2H2O | |
| D. | Fe3O4与稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
2.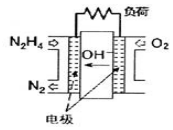 肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
 肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )| A. | 该电池放电时,通入肼的一极为负极 | |
| B. | 电池每释放1mol N2转移的电子数为4NA | |
| C. | 通入空气的一极的电极反应式是:O2+4e-+4H+=2H2O | |
| D. | 电池工作一段时间后,电解质溶液的pH将减小 |
12.X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期.下列说法正确的是( )
| A. | 简单离子半径R>W>Y>Z | |
| B. | 气态氢化物稳定性:HmW<HnR | |
| C. | Z2Y2电子式可表示为  | |
| D. | RY2和W2均有漂白性,将两者等物质的量混合溶于水,漂白性增强 |
19.某元素的原子最外层有2个电子,则这种元素是( )
| A. | 金属元素 | B. | 惰性气体元素 | C. | 第二主族元素 | D. | 以上叙述都可能 |
16.中和滴定中用已知浓度的稀盐酸滴定未知浓度的稀氨水,计算式与滴定氢氧化钠溶液类似:c1V1=c2V2,则( )
| A. | 终点溶液偏碱性 | B. | 终点溶液中c(NH4+)=c(Cl-) | ||
| C. | 终点溶液中氨过量 | D. | 合适的指示剂是甲基橙而非酚酞 |
17.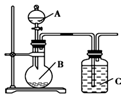 某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )
某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )
 某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )
某研究性学习小组根据元素非金属性与其最高价氧化物对应的水化物之间的关系,设计了如图装置来一次性完成S、C、Si的非金属性强弱比较的实验研究,下列关于试剂B选择正确的是( )| A. | 稀H2SO4 | B. | Na2SO4溶液 | C. | Na2CO3溶液 | D. | Na2SiO3溶液 |