题目内容
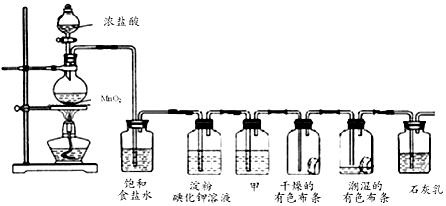
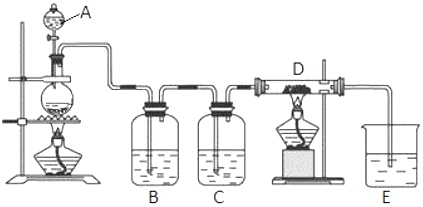
8.实验室用下列仪器和药品制取并收集干燥纯净的氯气.
(1)盛有浓盐酸的仪器名称是分液漏斗.
(2)按气流从左到右,装置正确的连接是:a 接(f)、(h)接(b )、( c )接(e )、(d)接( g )(填各接口字母)
(3)装置F 的作用是吸收氯化氢,装置B 的作用是吸收水干燥氯气.
(4)装置E 中发生反应的化学方程式是2NaOH+Cl2═NaCl+H2O+NaClO.
(5)装置A 中发生反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
分析 实验室用二氧化锰与浓盐酸加热制备氯气,浓盐酸易挥发,制备的氯气中含有氯化氢和水蒸气,依次通过盛有饱和食盐水、浓硫酸的洗气瓶除去杂质,氯气密度大于空气密度,用向上排气法收集,氯气有毒,过量的氯气应用氢氧化钠溶液吸收;
(1)依据仪器形状说出其名称;
(2)依据气体制备装置:发生装置、净化装置、收集装置、尾气吸收装置连接仪器;
(3)依据浓盐酸易挥发,制备的氯气中含有氯化氢和水蒸气,依据氯气、氯化氢、浓硫酸性质选择除杂剂;
(4)氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水;
(5)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水.
解答 解:(1)依据仪器形状可知盛放浓盐酸的仪器为:分液漏斗;
故答案为:分液漏斗;
(2)实验装置的连接顺序为:发生装置→除杂装置→收集装置→尾气处理装置;A为氯气的制取装置,浓盐酸与足量MnO2反应制取Cl2,反应需要加热,氯化氢易挥发,所以制取的氯气中含有水蒸气和氯化氢,由于氯气难溶于饱和食盐水,可用饱和食盐水除去氯化氢气体,然后用浓硫酸干燥得到了干燥、纯净的氯气,用向下排空气法收集氯气,最后要吸收多余的氯气,即仪器连接顺序为:a接f接h接b接c接e接d接g,
故答案为:f;h;e;d;
(3)制取氯气时需要加热,会使浓盐酸挥发出来,制取的氯气中含有氯化氢和水蒸气,Cl2不溶于饱和食盐水,而HCl溶于饱和食盐水,所以可以用装置F使用饱和食盐水除去HCl;浓硫酸具有吸水性,能够干燥氯气;
故答案为:吸收氯化氢;吸收水干燥氯气;
(4)氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水,方程式:2NaOH+Cl2═NaCl+H2O+NaClO;
故答案为:2NaOH+Cl2═NaCl+H2O+NaClO;
(5)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水,方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
点评 本题考查了实验室制取氯气,掌握实验室制备氯气的原理以及氯气的化学性质是解答的关键,题目难度不大,注意气体制备装置的一般连接顺序.

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案①由苯制取溴苯、硝基苯、环己烷的反应都属于取代反应
②铅蓄电池、锂电池、碱性锌锰电池都属于二次电池
③碳素钢、不锈钢和目前流通的硬币都属于合金
④浓盐酸、浓硫酸、浓硝酸都属于氧化性酸
⑤氨水、醋酸、氢氧化铝都属于弱电解质
⑥豆浆、淀粉水溶液、雾都属于胶体.
| A. | ③⑥ | B. | ①④ | C. | ②③⑥ | D. | ②④⑤ |
| A. | NH3是10电子微粒 | |
| B. | 氨气易液化,液氨可用作制冷剂 | |
| C. | 蘸有浓盐酸的玻璃棒遇氨气产生的白烟 | |
| D. | 氨气是电解质,NH3•H2O是非电解质 |
| A. | 300 mL0.1 mol/L NaCl溶液 | |
| B. | 100 mL0.1 mol/LFeCl3溶液 | |
| C. | 标准状况下,4.48LHC1气体溶于水配成的1 L溶液 | |
| D. | 向1 L0.2 mol/L BaCl2溶液中加入0.2 mol/L的H2SO4溶液到沉淀恰好完全时的溶液(忽略溶液混合时的体积变化) |
 的名称是2,2,4,5-四甲基-3,3-二乙基己烷
的名称是2,2,4,5-四甲基-3,3-二乙基己烷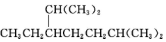 的名称为2,6-二甲基-3-乙基庚烷
的名称为2,6-二甲基-3-乙基庚烷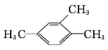 的名称是1,2,4-三甲苯
的名称是1,2,4-三甲苯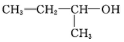 的名称是2-丁醇
的名称是2-丁醇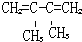 .
.
 混有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作,回答下列问题:
混有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作,回答下列问题: