题目内容
(1)在化学中,常用一条短线表示一个化学键,如图所示的物质结构中,虚线表示化学键或分子间作用力的是 (填序号).

(2)已知PH3与NH3结构相似,回答下列问题:
①PH3的电子式 ,结构式 .
②空间构型为 .
③中心原子采取 杂化.
④PH3分子中的化学键 (填“有”或“无”)极性,其分子为 (填“极性”或“非极性”)分子.
⑤PH3与NH3的热稳定性: 更强.

(2)已知PH3与NH3结构相似,回答下列问题:
①PH3的电子式
②空间构型为
③中心原子采取
④PH3分子中的化学键
⑤PH3与NH3的热稳定性:
考点:同一主族内元素性质递变规律与原子结构的关系,化学键和分子间作用力的区别
专题:
分析:(1)A、石墨晶体中同一层内原子以共价键结合,而层与层之间为范德华力;
B、白磷分子中,每个P原子形成3个共价键,达稳定结构;
C、在CCl4中,Cl原子之间的直线只是为了表示四个Cl原子形成的正四面体而已,不表示化学键;
D、立方烷中碳原子之间形成共价键;
(2)已知PH3与NH3结构相似,回答下列问题:
①PH3的电子式书写不能漏掉一对孤对电子对,结构式共用电子对用短线表示;
②空间构型为三角锥形;
③三个σ键和一个孤对电子对,所以中心原子采取sp3杂化.
④PH3分子中的化学键不同原子形成的共价键是极性键,其分子正负电荷中心不重合为极性分子;
⑤非金属性越强,氢化物越稳定,PH3与NH3的热稳定性:NH3 更强.
B、白磷分子中,每个P原子形成3个共价键,达稳定结构;
C、在CCl4中,Cl原子之间的直线只是为了表示四个Cl原子形成的正四面体而已,不表示化学键;
D、立方烷中碳原子之间形成共价键;
(2)已知PH3与NH3结构相似,回答下列问题:
①PH3的电子式书写不能漏掉一对孤对电子对,结构式共用电子对用短线表示;
②空间构型为三角锥形;
③三个σ键和一个孤对电子对,所以中心原子采取sp3杂化.
④PH3分子中的化学键不同原子形成的共价键是极性键,其分子正负电荷中心不重合为极性分子;
⑤非金属性越强,氢化物越稳定,PH3与NH3的热稳定性:NH3 更强.
解答:
解:(1)A、石墨晶体中同一层内原子以共价键结合,而层与层之间为范德华力,所以物质结构中实线表示化学键,虚线表示分子间作用力(范德华力),故A正确;
B、白磷分子中,每个P原子形成3个共价键,达稳定结构,所以物质结构中实线表示化学键,故B正确;
C、在CCl4中,Cl原子之间的直线只是为了表示四个Cl原子形成的正四面体而已,不表示化学键,故C错误;
D、立方烷中碳原子之间形成共价键,所以物质结构中实线表示化学键,故D正确;
故选:ABD;
(2)已知PH3与NH3结构相似,则
①PH3的电子式书写不能漏掉一对孤对电子,所以电子式为: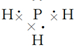 ,结构式共用电子对用短线表示,所以结构式为:
,结构式共用电子对用短线表示,所以结构式为: ,
,
故答案为: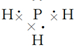 ;
; ;
;
②空间构型为三角锥形,故答案为:三角锥形;
③三个σ键和一个孤对电子对,所以中心原子采取sp3杂化,故答案为:sp3;
④PH3分子中的化学键不同原子形成的共价键是极性键,其分子正负电荷中心不重合为极性分子,故答案为:有;极性;
⑤非金属性越强,氢化物越稳定,PH3与NH3的热稳定性:NH3 更强,故答案为:NH3.
B、白磷分子中,每个P原子形成3个共价键,达稳定结构,所以物质结构中实线表示化学键,故B正确;
C、在CCl4中,Cl原子之间的直线只是为了表示四个Cl原子形成的正四面体而已,不表示化学键,故C错误;
D、立方烷中碳原子之间形成共价键,所以物质结构中实线表示化学键,故D正确;
故选:ABD;
(2)已知PH3与NH3结构相似,则
①PH3的电子式书写不能漏掉一对孤对电子,所以电子式为:
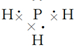 ,结构式共用电子对用短线表示,所以结构式为:
,结构式共用电子对用短线表示,所以结构式为: ,
,故答案为:
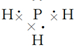 ;
; ;
; ②空间构型为三角锥形,故答案为:三角锥形;
③三个σ键和一个孤对电子对,所以中心原子采取sp3杂化,故答案为:sp3;
④PH3分子中的化学键不同原子形成的共价键是极性键,其分子正负电荷中心不重合为极性分子,故答案为:有;极性;
⑤非金属性越强,氢化物越稳定,PH3与NH3的热稳定性:NH3 更强,故答案为:NH3.
点评:本题考查物质结构、化学键、杂化方式、分子的空间构型等,综合性强,难度中等,注意物质空间结构图与键线式区别.

练习册系列答案
相关题目
下列关于金属的说法错误的是( )
| A、生铁和钢都是铁的合金 |
| B、铁在潮湿的空气中不会生锈 |
| C、铝表面有氧化保护膜 |
| D、在铁表面刷上油漆,可防止铁生锈 |
两种非金属元素A、B所形成的下列分子中属于非极性分子的是( )
A、 |
B、 |
C、 |
D、 |
共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量.如H-H键的键能是436KJ/mol,是指1molH2分子变成2molH原子需要吸收436KJ的能量.你认为下列分子中的共价键能量最大的是( )
| A、HF | B、HCl |
| C、HBr | D、HI |
等物质的量的氢气和氦气在同温同压下具有相等的( )
| A、原子数 | B、体积 |
| C、质子数 | D、质量 |