题目内容
5.向Ba(OH)2溶液中逐滴加入稀硫酸,溶液导电性的变化合理的图象为( )| A. | 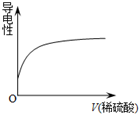 | B. | 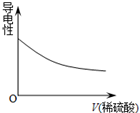 | C. | 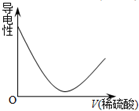 | D. | 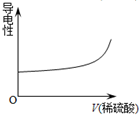 |
分析 电解质溶液的导电性与离子浓度成正比,溶液中离子浓度越大其导电能力越强,滴加过程中发生的反应为Ba(OH)2+H2SO4=BaSO4↓+2H2O,二者反应生成沉淀和弱电解质,导致溶液导电能力降低,据此分析解答.
解答 解:电解质溶液的导电性与离子浓度成正比,溶液中离子浓度越大其导电能力越强,滴加过程中发生的反应为Ba(OH)2+H2SO4=BaSO4↓+2H2O,滴入H2SO4时,导电性减弱,完全反应后,H2SO4过量,导电性又增强,故选C.
点评 本题考查电解质溶液导电性强弱判断,为高频考点,明确反应实质及溶液中溶质成分及其性质是解本题关键,注意电解质溶液导电性与电解质强弱无关,与离子浓度及离子所带电荷有关,为易错题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)
已知:
①A、B两溶液呈碱性;C、D、E溶液呈酸性.
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同).
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀.
试回答下列问题:
(1)分别写出A、E的化学式:ANa2CO3、EAl2(SO4)3
(2)写出A与E反应的离子方程式:2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓;
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H=-Q kJ•mol-1.写出B与C稀溶液反应的热化学方程式OH-(aq)+H+(aq)=H2O(1)△H=-QkJ/mol或$\frac{1}{2}$Ba(OH)2(aq)+HC1(aq)=$\frac{1}{2}$BaC12(aq)+H2O(1)△H=-QkJ/mol
或Ba(OH)2(aq)+2HC1(aq)=BaC12(aq)+2H2O(1)△H=-2QkJ/mol.
(4)在100mL 0.1mol•L-1 E溶液中,逐滴加入40mL 1.6mol•L-1 NaOH溶液,最终得到沉淀物质的量为0.016molmol.
| 阳离子 | H+ Na+ Al3+ Ag+ Ba2+ |
| 阴离子 | OH- Cl- CO32- NO3- SO42- |
①A、B两溶液呈碱性;C、D、E溶液呈酸性.
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同).
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀.
试回答下列问题:
(1)分别写出A、E的化学式:ANa2CO3、EAl2(SO4)3
(2)写出A与E反应的离子方程式:2Al3++3CO32-+3H2O═3CO2↑+2Al(OH)3↓;
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H=-Q kJ•mol-1.写出B与C稀溶液反应的热化学方程式OH-(aq)+H+(aq)=H2O(1)△H=-QkJ/mol或$\frac{1}{2}$Ba(OH)2(aq)+HC1(aq)=$\frac{1}{2}$BaC12(aq)+H2O(1)△H=-QkJ/mol
或Ba(OH)2(aq)+2HC1(aq)=BaC12(aq)+2H2O(1)△H=-2QkJ/mol.
(4)在100mL 0.1mol•L-1 E溶液中,逐滴加入40mL 1.6mol•L-1 NaOH溶液,最终得到沉淀物质的量为0.016molmol.
16.设阿伏伽德罗常数为NA,下列说法正确的是( )
| A. | 标准状况下,22.4L甲醛完全燃烧产生NA个CO2分子 | |
| B. | 1L1mol/L Na2CO3溶液中,阴离子个数等于NA | |
| C. | 100 g 98%的浓硫酸中含氧原子个数为4NA | |
| D. | 常温常压下,1mol白磷中含有共价键为4NA |
13.下列状态的物质,既属于电解质又能导电的是( )
| A. | 酒精 | B. | 熔融的氢氧化钠 | C. | 液氯 | D. | 氯化钾晶体 |
10.下列化合物中不属于有机物的是( )
| A. | 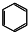 | B. | CH4 | C. | CH3CH2OH | D. | NH4CNO |
17.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| B. | 1.5molNO2与足量H2O反应,转移的电子数为1.5NA | |
| C. | 常温常压下,46gNO2和N2O4混合气体含有的原子数为3NA | |
| D. | 含有H2SO41mol的浓硫酸与足量铜反应,生成SO2的分子数为0.5NA |