题目内容
5.氮化铝(AlN)常用做砂轮及高温炉衬材料,熔化状态下不导电,可知它属于( )| A. | 离子晶体 | B. | 原子晶体 | C. | 分子晶体 | D. | 无法判断 |
分析 信息可知,氮化铝常用作砂轮及耐高温的材料,熔融时不导电为共价化合物,熔点高、硬度大,为原子晶体的性质,以此来解答.
解答 解:由信息可知,氮化铝常用作砂轮及耐高温的材料,熔融时不导电为共价化合物,由原子构成,熔点高、硬度大,为原子晶体的性质,所以氮化铝属于原子晶体;故B正确;故选B.
点评 本题考查晶体的判断,明确不同类型晶体的性质是解答本题的关键,难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
15.下列有关化学用语表示正确的是( )
| A. | 质量数为35的氯原子:${\;}_{35}^{17}$Cl | |
| B. | 14C的原子结构示意图: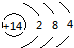 | |
| C. | N2分子的电子式: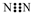 | |
| D. | 乙酸乙酯的结构简式为:CH3COOC2H5 |
16.有关化学键的说法正确的是( )
| A. | 全部由非金属元素构成的化合物一定是共价化合物 | |
| B. | 某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键一定是离子键 | |
| C. | 金属与非金属原子间只能形成离子键 | |
| D. | 含有共价键的化合物不一定是共价化合物 |
13.维生素C的结构简式为 ,丁香油酚的结构简式为:
,丁香油酚的结构简式为: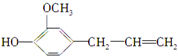 ,下列关于两者的说法正确的是( )
,下列关于两者的说法正确的是( )
 ,丁香油酚的结构简式为:
,丁香油酚的结构简式为: ,下列关于两者的说法正确的是( )
,下列关于两者的说法正确的是( )| A. | 均含酯基 | B. | 均含碳碳双键 | ||
| C. | 均含醇羟基和酚羟基 | D. | 均为芳香化合物 |
10.下列离子方程式的书写正确的是( )
| A. | 铁和稀硫酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 向硫酸钠溶液中滴加氯化钡溶液 Ba2++SO42-═BaSO4↓ | |
| C. | 氯水加入到溴化钾溶液中 Br-+Cl2═Br2+Cl- | |
| D. | 碳酸钙溶于稀盐酸 CO32-+2H+═H2O+CO2↑ |
17.某工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).下列对该产品的描述不正确的是( )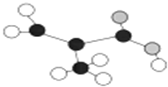

| A. | 官能团为碳碳双键、羧基 | B. | 与CH2=CHCOOCH3互为同分异构体 | ||
| C. | 能发生取代、加成和氧化反应 | D. | 分子中所有原子可能在同一平面 |
14.下列物质①乙烷②乙炔③甲苯④苯乙烯⑤聚乙烯⑥苯酚⑦乙醇,其中既能与溴水反应又能与酸性高锰酸钾溶液反应的是( )
| A. | ②③④⑤ | B. | ②④⑥ | C. | ②③④⑤⑥⑦ | D. | ②⑤⑥ |
15.下列过程中化学键没有被破坏的是( )
| A. | 水沸腾汽化 | B. | 水加热到1500℃开始分解 | ||
| C. | 氯化钠加热至熔化 | D. | NaOH固体溶于水 |
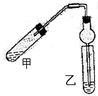 如图(铁架台、铁夹等省略)在试管甲中先加入碎瓷片,再加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上.在试管乙中加入5mL饱和碳酸钠溶液.按如图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验
如图(铁架台、铁夹等省略)在试管甲中先加入碎瓷片,再加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上.在试管乙中加入5mL饱和碳酸钠溶液.按如图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验