题目内容
已知有机物A是链状化合物,分子内只含有两种官能团,A和一些化学试剂的反应情况如图所示:
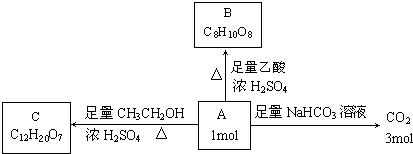
(1)A分子内含有的两种官能团是 、 ;A的分子式为 .
(2)核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境.则A的结构简式是 .
(3)由A生成B的化学方程式是 .

(1)A分子内含有的两种官能团是
(2)核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境.则A的结构简式是
(3)由A生成B的化学方程式是
考点:有机物的推断
专题:有机物的化学性质及推断
分析:根据流程图,1molA可以与碳酸氢钠溶液生成3mol二氧化碳,A中含有3个羧基;可以与醇发生酯化反应,A中含有羟基;根据形成的B、C两种酯的碳原子数,A中应该有6个碳原子,含一个羟基、3个羧基,分子中有4个氢处于完全相同的化学环境.则A的结构简式: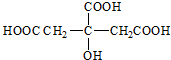 ,B的结构简式为
,B的结构简式为 ,C的结构简式为
,C的结构简式为 ,据此解答.
,据此解答.
 ,B的结构简式为
,B的结构简式为 ,C的结构简式为
,C的结构简式为 ,据此解答.
,据此解答.解答:
解:根据流程图,1molA可以与碳酸氢钠溶液生成3mol二氧化碳,A中含有3个羧基;可以与醇发生酯化反应,A中含有羟基;根据形成的B、C两种酯的碳原子数,A中应该有6个碳原子,含一个羟基、3个羧基,分子中有4个氢处于完全相同的化学环境.则A的结构简式: ,B的结构简式为
,B的结构简式为 ,C的结构简式为
,C的结构简式为 ,
,
(1)由上述分析可知,分子内含有的两种官能团是:羧基、羟基;根据A与乙酸反应生成BC8H10O8,结合原子守恒,则分子式为C6H8O7,
故答案为:羧基;羟基;C6H8O7;
(2)由上述分析可知,A的结构简式是 ,故答案为:
,故答案为: ;
;
(3)由A生成B的化学方程式是: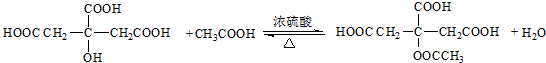 ,
,
故答案为: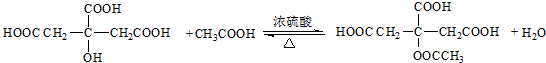 .
.
 ,B的结构简式为
,B的结构简式为 ,C的结构简式为
,C的结构简式为 ,
,(1)由上述分析可知,分子内含有的两种官能团是:羧基、羟基;根据A与乙酸反应生成BC8H10O8,结合原子守恒,则分子式为C6H8O7,
故答案为:羧基;羟基;C6H8O7;
(2)由上述分析可知,A的结构简式是
 ,故答案为:
,故答案为: ;
;(3)由A生成B的化学方程式是:
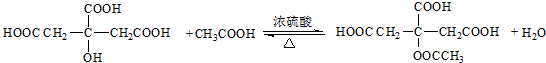 ,
,故答案为:
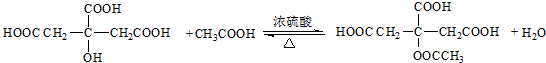 .
.
点评:本题考查有机物推断,综合分析A与酸、醇的酯化反应形成的酯分子式来判断A的碳原子数是解题的关键,难度中等.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列用来表示物质变化的化学用语中,正确的是( )
| A、NH4NO3溶液呈酸性的原因:NH4++H2O=NH3?H2O+H+ |
| B、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| C、硫酸氢钠溶液中滴加少量Ba(OH)2溶液的离子方程式:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓ |
D、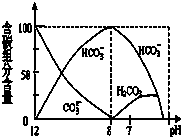 如图是在0.1 mol?L-1Na2CO3溶液中逐滴加入0.1 mol?L-1 HCl,则 pH=7时的离子方程式:H++HCO3-=CO2↑+H2O |
某一有机物A(C8H16O2)可发生如图变化;已知B为羧酸,且D氧化可以得到B,则A的可能结构有( )
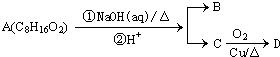
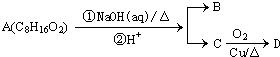
| A、1种 | B、2种 | C、3种 | D、4种 |
微观粒子是化学研究的主要对象.若阿伏加德罗常数为6.02×1023mol-1,下列对粒子数判断正确的是( )
| A、常温常压下,2.24L H2O2气体中含有的分子数为0.1×6.02×1023 |
| B、46 g NO2和N2O4混合气体中含有原子数为3NA |
| C、100 mL 0.2 mol/L的Fe2(SO4)3溶液中,含有的Fe3+数为0.1×0.2×6.02×1023 |
| D、25℃时,纯水中含有的H+数为1×10-7×6.02×1023 |
 A、B、C、D、E为五种原子序数逐渐增大的短周期元素,其中 A与B组成的化合物是一种温室气体,B与D、C与D组成的化合物是机动车排出的大气污染物,D和E能形成原子个数比为1:1和1:2的两种离子化合物.
A、B、C、D、E为五种原子序数逐渐增大的短周期元素,其中 A与B组成的化合物是一种温室气体,B与D、C与D组成的化合物是机动车排出的大气污染物,D和E能形成原子个数比为1:1和1:2的两种离子化合物.