题目内容
干燥剂的干燥性能可用干燥效率(1m3空气中实际余留水蒸气的质量)来衡量.某些干燥剂的干燥效率数据如下分析以上数据,下列有关叙述错误的是.( )
| 物质 | 干燥效率 | 物质 | 干燥效率 |
| MgO | 0.008 | ZnCl2 | 0.8 |
| CaO | 0.2 | ZnBr2 | 1.1 |
| A、MgO的干燥性能比CaO好 |
| B、干燥效率可能与干燥剂的阴、阳离子的半径大小有关 |
| C、MgCl2可能是比CaCl2更好的干燥剂 |
| D、上述干燥剂中阳离子对干燥剂性能的影响比阴离子小 |
考点:微粒半径大小的比较
专题:信息给予题
分析:A.MgO的干燥效率好;
B.镁离子比钙离子半径小,氯离子比溴离子半径小,构成阳离子和阴离子的半径越小,干燥性能越好;
C.构成阳离子和阴离子的半径越小,干燥性能越好;
D.阳离子的改变对干燥性能影响大.
B.镁离子比钙离子半径小,氯离子比溴离子半径小,构成阳离子和阴离子的半径越小,干燥性能越好;
C.构成阳离子和阴离子的半径越小,干燥性能越好;
D.阳离子的改变对干燥性能影响大.
解答:
解:A.干燥效率是:1m3空气中实际余留水蒸气的质量,MgO为0.008,CaO为0.2,即有MgO的1m3空气中实际余留水蒸气的质量更少,MgO的干燥效率比CaO好,故A正确;
B.构成阳离子和阴离子的半径越小,干燥性能越好,则干燥效率可能与干燥剂的阴、阳离子的半径大小有关,故B正确;
C.镁离子比钙离子半径小,氯离子比溴离子半径小,MgCl2比CaCl2干燥性能更好,故C正确;
D.对比表中阴阳离子变化的干燥效率数值,阳离子改变干燥效率变化大,阴离子改变干燥效率变化小,故D错误.
故选:D.
B.构成阳离子和阴离子的半径越小,干燥性能越好,则干燥效率可能与干燥剂的阴、阳离子的半径大小有关,故B正确;
C.镁离子比钙离子半径小,氯离子比溴离子半径小,MgCl2比CaCl2干燥性能更好,故C正确;
D.对比表中阴阳离子变化的干燥效率数值,阳离子改变干燥效率变化大,阴离子改变干燥效率变化小,故D错误.
故选:D.
点评:本题属于信息给予题,题目难度不大,通过阅读题干理解干燥效率的含义,通过表中的物质的组成和干燥效率关系,比较、分析获得结论,侧重于考查学生分析问题和解决问题的能力.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
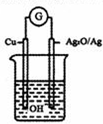 普通水泥在固化过程中自由水分子减少并形成碱性溶液,根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag.下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并形成碱性溶液,根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间.此法的原理,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag.下列有关说法正确的是( )| A、铜电极附近有黑色沉淀生成 |
| B、负极的电极反应式为2Cu+2OH--2e-═Cu2O+H2O |
| C、测量原理示意图中,电流方向从Cu经过导线流向Ag2O |
| D、电池工作时,溶液中OH-向正极移动 |
下列依据相关数据作出的推理和判断中,不正确的是( )
| A、依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低 |
| B、依据溶解度的数据,选择用重结晶的方法可将粗苯甲酸提纯 |
| C、依据沸点的数据,判断用分馏的方法从石油中获取汽油和煤油等 |
| D、依据燃烧热的数据、热化学方程式和盖斯定律,可计算一些反应的反应热 |
卤素单质F2、Cl2、Br2、I2的密度的变化规律是( )
| A、逐渐增大 | B、逐渐减小 |
| C、不变 | D、没有规律 |
如图为元素周期表短周期的一部分.下列关于A~F六种元素的叙述正确的是( )

| A、A、B、D、E四种元素所形成的最高价含氧酸中D的酸性最强 |
| B、形成的简单阴离子半径的大小顺序为:C>B>D>E |
| C、D、E、F三种元素形成的单质中都含有共价键 |
| D、1 mo1A、B、C元素的简单氢化物中都含有10 mol电子 |
碱金属元素钠的电子层数是( )
| A、一层 | B、二层 | C、三层 | D、四层 |
1L0.1mol?L-1 AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极增重2.16g时,下列判断正确的是(设电解按理论进行,溶液不蒸发)( )
| A、转移的电子数是1.204×1022 |
| B、阳极上产生112mLO2(标准状况) |
| C、溶液的浓度变化为0.08mol?L-1 |
| D、反应中有0.01molAg被氧化 |
 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )| A、AB段发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ |
| B、E点对应横坐标稀硫酸的体积为70 mL |
| C、D点表示的沉淀的化学式为Al(OH)3、BaSO4 |
| D、E点沉淀比A点沉淀质量大2.33g |
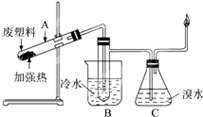 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如下表
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如下表