题目内容
9.某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程中,除了生成NO2气体外,还会有少量NO生成,并测定Cu、Ag合金中Cu的质量分数.查阅相关资料表明:“常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在.”为此,他们设计了如图所示的装置:
请回答下列问题:
(1)写出A中Cu与HNO3反应可能的化学方程式Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O.
(2)实验开始前先打开A部分的活塞K1,持续通入一段时间的氮气再关闭K1,其目的是排出系统的空气,防止NO氧化为NO2;装置中B瓶的作用是吸收水蒸气,防止水蒸气在C中冷凝后与NO2反应产生NO.
(3)停止反应后,打开D中的活塞K2并通入O2,则D中能出现的现象是无色气体变成红棕色气体.
(4)C装置的作用是尽量把NO2转化为N2O4,减少对NO检验的干扰;E装置的作用是除去NO2,防止污染空气.
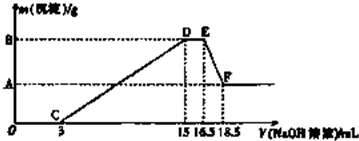
(5)若A中的Cu、Ag合金的质量为8.0g,加入20mL 13.5mol•L-1的浓HNO3,实验结束后A中溶液的体积不变,测得 c (H+)=1.0mol•L-1.假设反应中HNO3既无挥发也无分解,则参加反应的HNO3的物质的量为0.25mol.
(6)若已知Cu、Ag合金的质量为m g,且溶解完全.请利用A装置中反应后的溶液进行简单的操作,以确定合金中Cu的质量分数,其实验过程为在A中加入过量的Cl-的溶液,过滤、洗涤、干燥并称量沉淀的质量.
分析 实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,排尽装置中的空气,滴入浓硝酸反应生成二氧化氮和一氧化氮气体,干燥后通过装置C,在低于0℃时几乎只有无色的N2O4液体或晶体存在,A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO产生,则D中出现红棕色气体,说明有一氧化氮气体生成,剩余气体用氢氧化钠溶液吸收;
(1)根据铜和浓硝酸反应生成二氧化氮、硝酸铜和水,随着反应的进行,硝酸浓度变稀,铜和稀硝酸反应生成一氧化氮气体,硝酸铜和水;
(2)通入氮气是排除装置中的空气,避免生成的一氧化氮气体被氧化为二氧化氮;B装置是利用浓硫酸的吸水性吸收气体中的水蒸气避免在C中 冷却后水和二氧化氮反应生成一氧化氮;
(3)一氧化氮和氧气反应生成红棕色二氧化氮气体;
(4)C装置是冷却气体使二氧化氮转化为四氧化二氮减少NO检验的干扰,E装置除去尾气防止倒吸、防止污染空气;
(5)硝酸的总的物质的量n=13.5mol•L1×0.04L=0.54mol,剩余硝酸n=1mol•L1×0.04L=0.04mol,确定反应的硝酸的物质的量;
(6)铜银合金和硝酸全部反应生成铜盐和银盐,利用A装置中银离子和氯离子形成的沉淀称量计算得到合金中铜的质量分数.
解答 解:(1)铜和浓硝酸反应生成二氧化氮、硝酸铜和水,随着反应的进行,硝酸浓度变稀,铜和稀硝酸反应生成一氧化氮气体,硝酸铜和水,反应的可能化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
(2)通入氮气是排出装置中的空气,避免生成的一氧化氮气体被氧化为二氧化氮;B装置是利用浓硫酸的吸水性吸收气体中的水蒸气避免在C中冷却后水和二氧化氮反应生成一氧化氮,
故答案为:排出系统的空气,防止NO氧化为NO2;吸收水蒸气,防止水蒸气在C中冷凝后与NO2反应产生NO;
(3)A中的反应停止后,打开D中的活塞K2再通入氧气,若反应中确有NO产生,一氧化氮和氧气反应生成红棕色气体二氧化氮气体;
故答案为:无色气体变成红棕色气体;
(4)C装置是冷却气体使二氧化氮转化为四氧化二氮,尽量把NO2转化为N2O4,减少对NO检验的干扰,E装置除去尾气NO2防止倒吸、防止污染空气;
故答案为:尽量把NO2转化为N2O4,减少对NO检验的干扰;除去NO2,防止污染空气;
(5)硝酸的总的物质的量n=13.5mol•L1×0.02L=0.27mol,剩余硝酸n=1mol•L1×0.02L=0.02mol,所以参加反应的硝酸是0.27mol-0.02mol=0.25mol;
故答案为:0.25mol;
(6)铜银合金和硝酸全部反应生成铜盐和银盐,利用A装置中银离子和氯离子形成的氯化银沉淀称量,即在A中加入过量的Cl-的溶液,过滤、洗涤、干燥并称量沉淀的质量,从而计算得到合金中铜的质量分数,
故答案为:在A中加入过量的Cl-的溶液,过滤、洗涤、干燥并称量沉淀的质量.
点评 本题考查了物质性质的实验设计,涉及硝酸性质,实验步骤和产物性质及其反应现象是解题关键,题目难度中等.

| A. | CH2Br-CH2Br 二溴乙烷 | B. | CH3OOCCH3乙酸甲酯 | ||
| C. |  硬脂酸甘油脂 硬脂酸甘油脂 | D. | 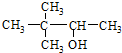 2,2-二甲基-3-丁醇 2,2-二甲基-3-丁醇 |
①浓硫酸和浓盐酸在空气中敞口放置时浓度均减小
②二氧化硫和氯气均能使品红溶液褪色
③二氧化硫能使品红溶液、溴水褪色
④氨气和碘化氢气体均不能用浓硫酸干燥
⑤常温下浓硫酸用铁制容器存放、加热条件下浓硫酸能与木炭反应
⑥浓硫酸能在白纸上写字,氢氟酸能在玻璃上刻字
⑦二氧化碳、二氧化硫使澄清石灰水变混浊.
| A. | 只有②④⑤ | B. | 只有⑤⑦ | C. | 只有①③⑦ | D. | 只有①② |
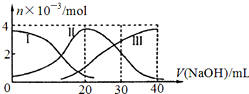
| A. | H2 A在水中的电离方程式是:H2A=H ++HA -;HA -═H++A2- | |
| B. | 当V(NaOH)=20mL时,则有:c(Na + )>c(HA- )>c(H + )>c(A 2- )>c(OH- ) | |
| C. | 当V(NaOH)=30mL时,则有:2c(H + )+c(HA- )+2c(H2A)=c(A 2- )+2 c(OH- ) | |
| D. | 当V(NaOH)=40mL时,其溶液中水的电离受到抑制 |
| A. | CH3CH2Br$→_{水}^{NaOH}$ CH3CH2OH$→_{170℃}^{浓硫酸}$ CH2=CH2$\stackrel{Br_{2}}{→}$ CH2BrCH2Br | |
| B. | CH3CH2Br $\stackrel{HBr}{→}$ CH2BrCH2Br | |
| C. | CH3CH2Br $→_{水}^{NaOH}$ CH2=CH2 CH2BrCH3$\stackrel{HBr_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br $→_{醇}^{NaOH}$ CH2=CH2$\stackrel{Br_{2}}{→}$ CH2BrCH2Br |
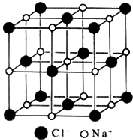
| A. | 在NaCl晶体中,每个Na+周围与其距离最近的Na+有6个 | |
| B. | 氯离子采取A2密堆积,钠离子填入八面体空隙中 | |
| C. | 每个晶胞含2个Na+和2个Cl- | |
| D. | 氯化钠的化学式为NaCl |