题目内容
下列实验装置设计正确且能达到相应实验目的是( )
A、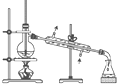 石油分馏 |
B、 制备乙酸乙酯 |
C、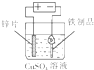 铁制品表面镀锌 |
D、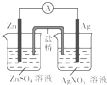 构成银锌原电池 |
考点:化学实验方案的评价,原电池和电解池的工作原理,石油的分馏,乙酸乙酯的制取
专题:实验评价题
分析:A.温度计水银球与蒸馏烧瓶支管口处相平;
B.应用饱和碳酸钠吸收;
C.用含待镀金属离子溶液做电解质溶液;
D.原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
B.应用饱和碳酸钠吸收;
C.用含待镀金属离子溶液做电解质溶液;
D.原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
解答:
解:A.温度计水银球与蒸馏烧瓶支管口处相平,温度计测得温度应是气体的温度,故A错误;
B.应用饱和碳酸钠吸收乙醇,除去乙酸,降低乙酸乙酯的溶解度,不能用氢氧化钠,故B错误;
C.用含待镀金属离子溶液做电解质溶液,应用硫酸锌,故C错误;
D.该装置符合原电池的构成条件,属于原电池,锌易失电子作负极,银作正极,故D正确.
故选D.
B.应用饱和碳酸钠吸收乙醇,除去乙酸,降低乙酸乙酯的溶解度,不能用氢氧化钠,故B错误;
C.用含待镀金属离子溶液做电解质溶液,应用硫酸锌,故C错误;
D.该装置符合原电池的构成条件,属于原电池,锌易失电子作负极,银作正极,故D正确.
故选D.
点评:本题考查化学实验方案评价,涉及物质的分离提纯、乙酸乙酯的制取、电镀和原电池等实验,侧重实验原理及物质性质的考查,注意从实验的合理性、可操作性等方面分析,题目难度中等.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为193K,沸点为411K,遇水很容易反应,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得.下列有关说法不正确的是( )
| A、S2C12晶体中不存在离子键 |
| B、S2C12分子中各原子均达到8电子稳定结构 |
| C、S2C12在液态下不能导电 |
| D、制备S2C12的反应是化合反应,不是氧化还原反应 |
下列物质中都含有氢元素,按照已学知识判断其中属于酸的是( )
| A、NH3 |
| B、HCl |
| C、NaHCO3 |
| D、CH4 |
某无色透明溶液与铝反应放出氢气,该溶液中可能存在下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、SO32-、HCO3-、OH-、
NO3-中的几种,下列情况正确的是( )
NO3-中的几种,下列情况正确的是( )
| A、当溶液中有Al3+生成时,溶液中可能存在:SO42-、NO3-、H+、Mg2+ |
| B、当溶液中有Al3+生成时,溶液中一定存在H+、SO42-,可能存在Mg2+ |
| C、当溶液中有AlO2-生成时,溶液中一定存在:OH-、Ba2+、NO3- |
| D、当溶液中有AlO2-生成时,溶液中可能存在:OH-、Ba2+、NO3-、SO32- |
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法不正确的是( )


| A、工业上通过电解熔融状态MgCl2制取金属镁 |
| B、用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C、在第②、④步骤中,溴元素均被氧化 |
| D、制取NaHCO3的反应是利用其溶解度小于NaCl |



