题目内容
将0.1 L含有0.02mol CuSO4和0.01molNaCl的水溶液用惰性电极电解。电解一段时间后,一个电极上得到0.01 mol Cu,另一电极析出的气体
A.只有Cl2 B.只有O2 C.既有Cl2又有O2 D.只有H2
C
【解析】
试题分析:溶液中含有n(Cu2+)=0.02mol,n(Cl-)=0.01mol;用惰性电极电解,电解一段时间后,一个电极上得到0.01mol Cu,是阴极反应,另一电极析出的气体为阳极反应;发生的电极反应为:阳极电极反应:2Cl--2e-=Cl2↑;根据得到铜物质的量计算电子转移,阳极电子转移守恒分析判断离子反应情况;阳极电极反应:2Cl- - 2e- =Cl2↑;
0.01mol 0.01mol
4OH- - 4e-= 2H2O+O2↑
0.01mol 0.01mol
阴极电极反应:Cu2++2e-=Cu;
0.02mol 0.01mol
依据上述分析和计算得到,阳极反应生成的气体是氧气和氯气;答案选C。
考点:考查原电池和电解池的工作原理。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
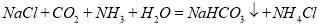 ”是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是
”是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是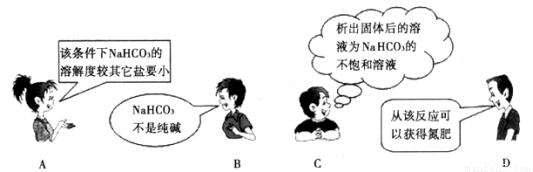

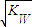 mol·L·-1
mol·L·-1