题目内容
(1)氯化铁水解的离子方程式为 ,配制氯化铁溶液时滴加少量盐酸的作用是 ;
(2)若向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐逐渐溶解,并产生无色气体,其离子方程式为 ,同时有红褐色沉淀生成的原因是 .
(2)若向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐逐渐溶解,并产生无色气体,其离子方程式为
考点:盐类水解的应用
专题:盐类的水解专题
分析:(1)氯化铁为强酸弱碱盐,水解呈酸性,配制溶液时应防止水解生成沉淀而使溶液变浑浊;
(2)氯化铁水解呈酸性,可使碳酸钙溶解,以此解答.
(2)氯化铁水解呈酸性,可使碳酸钙溶解,以此解答.
解答:
解:(1)氯化铁为强酸弱碱盐,水解呈酸性,水解离子方程式为Fe3++3H2O≒Fe(OH)3+3H+,配制溶液时应防止水解生成沉淀而使溶液变浑浊,则应加入盐酸,
故答案为:Fe3++3H2O≒Fe(OH)3+3H+;抑制氯化铁的水解;
(2)氯化铁水解呈酸性,可使碳酸钙溶解,反应的方程式为CaCO3+2H+=Ca2++H2O+CO2↑,反应消耗H+,使c(H+)减小,引起水解平衡向右移动,导致Fe(OH)3增多,形成红褐色沉淀,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑; CaCO3与上述水解平衡中的H+反应,使c(H+)减小,引起水解平衡向右移动,导致Fe(OH)3增多,形成红褐色沉淀.
故答案为:Fe3++3H2O≒Fe(OH)3+3H+;抑制氯化铁的水解;
(2)氯化铁水解呈酸性,可使碳酸钙溶解,反应的方程式为CaCO3+2H+=Ca2++H2O+CO2↑,反应消耗H+,使c(H+)减小,引起水解平衡向右移动,导致Fe(OH)3增多,形成红褐色沉淀,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑; CaCO3与上述水解平衡中的H+反应,使c(H+)减小,引起水解平衡向右移动,导致Fe(OH)3增多,形成红褐色沉淀.
点评:本题考查盐类水解的应用,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意盐类水解的原理是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
下列有关实验的叙述正确的是( )
| A、在硅酸钠溶液中滴入稀盐酸,溶液变浑浊,说明Cl元素的非金属性强于Si元素 |
| B、Zn与稀硫酸反应时,滴加少量CuSO4溶液,反应速率加快,说明CuSO4在该反应中起催化剂作用 |
| C、用酚酞作指示剂,盐酸滴定Na2CO3溶液,达到滴定终点时,离子浓度关系为:c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+) |
| D、将NaAlO2溶液与NaHCO3溶液混合,出现白色沉淀,是两种溶液水解相互促进的结果 |
下列各组物质中,所含分子数相同的是( )
| A、9 g H2O和0.5molBr2 |
| B、5.6LN2(标准状态)和11 g CO2 |
| C、10 g H2和10 g O2 |
| D、224mlH2(标准状态) 和0.1molN2 |
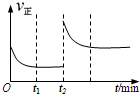 一定温度下,在一个10L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=
一定温度下,在一个10L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=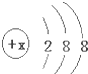 有几种元素的微粒的最外电子层结构如图所示,其中:
有几种元素的微粒的最外电子层结构如图所示,其中: