题目内容
将34.2g C12H22O11(蔗糖)溶解在100mL水中.关于所组成的溶液,下列叙述中正确的是( )
分析:由n=
可知,34.2g C12H22O11(蔗糖)的物质的量为0.1mol,但溶液的体积不是0.1L,以此来解答.
| m |
| M |
解答:解:A.n(C12H22O11)=
=0.1mol,由c=
可计算浓度,但溶解在100mL水中溶液的体积不是0.1L,则浓度不是1mol/L,故A错误;
B.由溶质的质量和溶液的质量可计算质量分数,则该溶液溶质的质量分数为
×100%,故B正确;
C.由B及c=
可知,该溶液中溶质的物质的量浓度的确定还需知道溶液的密度,故C正确;
D.由B和C可知,质量分数可直接计算,故D错误;
故选BC.
| 34.2g |
| 342g/mol |
| n |
| V |
B.由溶质的质量和溶液的质量可计算质量分数,则该溶液溶质的质量分数为
| 34.2g |
| 134.2g |
C.由B及c=
| 1000ρw |
| M |
D.由B和C可知,质量分数可直接计算,故D错误;
故选BC.
点评:本题考查物质的量浓度、质量分数的计算,明确换算公式及基本计算公式即可解答,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
将34.2g C12H22O11(蔗糖)溶解在100 mL水中。关于所组成的溶液,下列叙述中正确的是
|
A.该溶液中溶质的物质的量浓度为1 mol·L-1 |
|
B.该溶液溶质的质量分数为×100% |
|
C.该溶液中溶质的物质的量浓度的确定还需知道溶液的密度 |
|
D.该溶液溶质的质量分数的确定还需知道溶液的密度 |
将34.2g C12H22O11(蔗糖)溶解在100 mL水中。关于所组成的溶液,下列叙述中正确的是
| A.该溶液中溶质的物质的量浓度为1 mol·L-1 |
| B.该溶液溶质的质量分数为×100% |
| C.该溶液中溶质的物质的量浓度的确定还需知道溶液的密度 |
| D.该溶液溶质的质量分数的确定还需知道溶液的密度 |
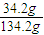 ×100%
×100%