题目内容
3.Na2CO3和NaHCO3是金属钠常见的两种碳酸盐,它们广泛地应用于生产和生活中.下列有关碳酸钠和碳酸氢钠的说法中,不正确的是( )| A. | NaHCO3能中和胃酸,对胃壁不产生强烈的刺激或腐蚀作用,可用于治疗胃酸过多症,但不适合胃溃疡病人 | |
| B. | NaHCO3能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头 | |
| C. | Na2CO3溶液中混有NaHCO3时,用给溶液加热的方法不能除去 | |
| D. | 往Na2CO3饱和溶液中通入CO2气体,可获得NaHCO3沉淀,由此可说明Na2CO3的溶解度比NaHCO3大 |
分析 A、小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗;
B、NaHCO3与酸反应生成二氧化碳气体;
C、Na2CO3溶液中混有NaHCO3时,加入适量的氢氧化钠,使碳酸氢钠转化为碳酸钠;
D、Na2CO3比NaHCO3易溶于水.
解答 解:A.小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗,因为反应产生的二氧化碳气体会造成胃部气胀,易造成胃穿孔,故A正确;
B、NaHCO3与酸反应生成二氧化碳气体,遇热膨胀而形成小孔,使得馒头或面包暄软多空,故B正确;
C、Na2CO3溶液中混有NaHCO3时,加入适量的氢氧化钠,使碳酸氢钠转化为碳酸钠,而不是加热,故C正确;
D、Na2CO3比NaHCO3易溶于水,在饱和Na2CO3溶液中通入过量二氧化碳气体可得到NaHCO3沉淀,则往两者饱和溶液中通入CO2,最终会形成澄清溶液的是NaHCO3,故D错误;
故选D.
点评 本题考查Na2CO3和NaHCO3性质的异同,侧重于学生的分析能力的考查,为高频考点,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列说法不正确的是( )
| A. | (CH3)2C═O+HCN→(CH3)2C(OH)CN 属于加成反应 | |
| B. | CH3OH、CH2OHCH2OH、CH2OHCHOHCH2OH是同系物 | |
| C. |  属于取代反应 属于取代反应 | |
| D. | 1molCH3CH3与Cl2完全反应生成六氯乙烷时,消耗Cl26mol |
18.在恒温、体积为2L的密闭容器中加入1molCO2和3molH2,发生如下的反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0.
可认定该可逆反应在一定条件下已达到化学平衡状态的是( )
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0.
可认定该可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | 容器中CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1 | |
| B. | v正(CO2)=3v逆(H2) | |
| C. | 容器内混合气体平均相对分子质量保持不变 | |
| D. | 容器中CO2、H2、CH3OH、H2O的物质的量浓度都相等 |
8.下列有机实验操作或叙述正确的是( )
| A. | 实验室配制银氨溶液时,应将2%硝酸银滴入2mL 2%的氨水中 | |
| B. | 除去乙酸乙酯中的部分乙醇和乙酸可用饱和Na2CO3溶液 | |
| C. | 卤代烃和酯的水解都可用浓硫酸作催化剂 | |
| D. | 在卤代烃水解后的溶液中加入硝酸银溶液观察沉淀现象就可确定其中的卤素 |
15.从海带中提取碘单质,成熟的工艺流程如下:干海带$\stackrel{灼烧}{→}$海带灰$→_{浸泡}^{沸水}$悬浊液$\stackrel{过滤}{→}$滤液$→_{H_{2}O_{2}}^{H+}$碘水$\stackrel{CCl_{4}}{→}$I2的CCl4
溶液$\stackrel{蒸馏}{→}$ I2下列关于海水制碘的说法正确的是( )
溶液$\stackrel{蒸馏}{→}$ I2下列关于海水制碘的说法正确的是( )
| A. | 实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌 | |
| B. | 含I-的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 | |
| C. | 在碘水中加入几滴淀粉溶液,溶液出现蓝色沉淀 | |
| D. | 碘水加入CCl4得到I2的CCl4溶液,该操作为萃取 |
13.下列叙述正确的是( )
| A. | 聚氯乙烯与乙烯性质相似,可使溴水褪色 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | C5H11Cl有8种同分异构体 | |
| D. | 相同条件下,熔沸点:正丁烷<异丁烷 |
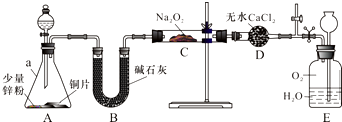
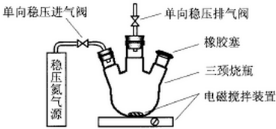 水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg/L.某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO.
水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg/L.某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO.