题目内容
15.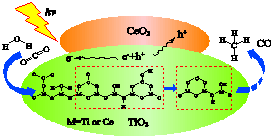 2016年3月新疆理化技术研究所首先发现:在光、碱性CeO2修饰TiO2的复合纳米材料的催化作用下,二氧化碳和水可转化为甲烷和一氧化碳.下列说法不正确的是( )
2016年3月新疆理化技术研究所首先发现:在光、碱性CeO2修饰TiO2的复合纳米材料的催化作用下,二氧化碳和水可转化为甲烷和一氧化碳.下列说法不正确的是( )| A. | 此反应可将光能转化为化学能 | |
| B. | CO2和CH4均含极性共价键 | |
| C. | 产物可能还有O2 | |
| D. | CO2溶于水呈酸性的原因:CO2+H2O?H2CO3H2CO3?2H++CO32- |
分析 A.由反应条件判断能量的变化;
B.不同种元素的原子之间形成的共价键为极性共价键;
C.水在光照、催化剂条件下分解氢气和氧气;
D.碳酸是弱酸,分步电离.
解答 解:A.在光、碱性CeO2修饰TiO2的复合纳米材料的催化作用下,二氧化碳和水可转化为甲烷和一氧化碳,该反应将光能转化为化学能,故A正确;
B.CO2和CH4中分别含有C=O、C-H,都是不同种元素的原子之间形成的共价键,都是极性共价键,故B正确;
C.水在光照、催化剂条件下分解氢气和氧气,所以产物可能有O2,故C正确;
D.碳酸电离方程式为H2CO3?H++HCO3-,HCO3-?H++CO32-,故D错误;
故选D.
点评 本题考查常见能量转化形式,涉及化学键的类型、水的光解、弱酸电离方程式的书写等知识,题目难度不大.

练习册系列答案
相关题目
6.现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.
回答下列问题:
(1)①在元素周期表中的位置是(周期、族)第二周期第VIA族.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式是: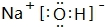 .
.
(3)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:Mg(OH)2+2H+=Mg2++2H2O.
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)①在元素周期表中的位置是(周期、族)第二周期第VIA族.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式是:
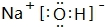 .
.(3)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:Mg(OH)2+2H+=Mg2++2H2O.
8.下列表述正确的是( )
| A. | 二氧化硫、氨、煤的液化均为物理变化 | |
| B. | 2CH3CH2OD+O2$→_{△}^{Cu}$2CH3CHO+2DHO | |
| C. | 甲醇、乙二醇、丙三醇都为饱和醇,熔沸点依次降低 | |
| D. | 已知常温下氢氧化镁的溶度积常数为a,则氢氧化镁悬浊液中:c(OH-)=$\root{3}{a}$mol/L |
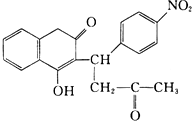
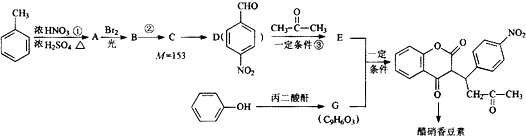
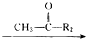 R1-CH═
R1-CH═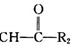 +H2O
+H2O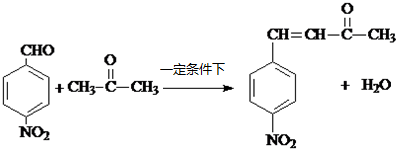 .
.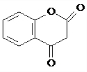 .
.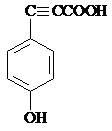 .
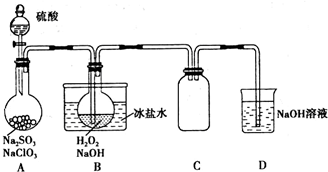
.
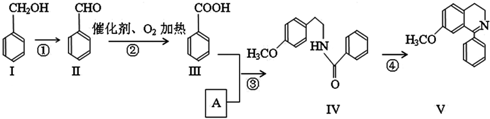
 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2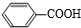
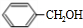 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O
+H2O
 .
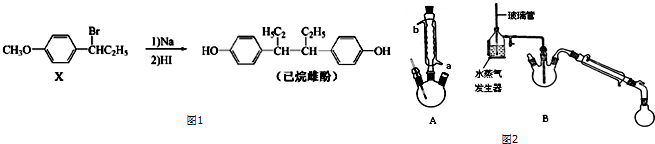
.
 .
.