题目内容
8.有一包白色粉末,其中可能含有NaNO3、CaCl2、K2CO3.现做以下实验:①将部分粉末加入水中,振荡,有白色沉淀生成;
②向①的悬浊液中加入过量稀硝酸,振荡,白色沉淀消失并有气泡产生;
③取少量②的溶液滴入AgNO3溶液,有白色沉淀生成.
根据上述实验现象,完成下列各题:
(1)原白色粉末中肯定含有的物质为CaCl2与K2CO3.
(2)写出步骤②中发生反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O.
分析 由①将部分粉末加入水中,振荡,有白色沉淀生成,白色沉淀为碳酸钙,一定含CaCl2、K2CO3;
②向①的悬浊液中加入过量稀硝酸,振荡,白色同淀消失并有气泡产生,碳酸钙溶于硝酸生成二氧化碳气体;
③取少量②的溶液滴入AgNO3溶液,有白色沉淀生成,白色沉淀为AgCl,以此来解答.
解答 解:由①将部分粉末加入水中,振荡,有白色沉淀生成,白色沉淀为碳酸钙,一定含CaCl2、K2CO3;
②向①的悬浊液中加入过量稀硝酸,振荡,白色同淀消失并有气泡产生,碳酸钙溶于硝酸生成二氧化碳气体,原固体一定含K2CO3;
③取少量②的溶液滴入AgNO3溶液,有白色沉淀生成,白色沉淀为AgCl,原固体一定含CaCl2,
(1)由上述分析可知,原白色粉末中肯定含有的物质为CaCl2与 K2CO3,故答案为:CaCl2与 K2CO3;
(2)步骤②中发生反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O,故答案为:CaCO3+2H+═Ca2++CO2↑+H2O.
点评 本题考查物质的组成的推断,为高频考点,把握物质的性质、发生的反应和现象为解答的关键,侧重分析与推断能力的考查,题目难度不大.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
16.下列说法不正确的是( )
| A. | 用铜作电极电解NaCl溶液,可以实现反应:Cu+2H2O$\frac{\underline{\;电解\;}}{\;}$Cu(OH)2↓+H2↑ | |
| B. | 用铜、铝作电极与电解质溶液构成原电池时,铜一定是正极 | |
| C. | N2O4和NO2混合气体69g,完全与水反应转移电子数约为6.02×1023 | |
| D. | HCl和HS-均是含有一个极性键的18电子粒子 |
20.检验溴乙烷中是否有溴元素,合理的实验方法是( )
| A. | 加入氯水后振荡,看水层里是否有棕红色的溴出现 | |
| B. | 加入硝酸银溶液,再加稀硝酸,观察有无浅黄色沉淀生成 | |
| C. | 加入NaOH水溶液共热,冷却后加硝酸银溶液,观察有无浅黄色沉淀生成 | |
| D. | 加入NaOH水溶液共热,冷却后用过量稀硝酸中和过量碱后,再加硝酸银溶液,观察有无浅黄色沉淀生成 |
17.下列有关物质的制备或保存方法正确的是( )
| A. | 实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 | |
| B. | 氢氧化钠溶液保存在玻璃塞的试剂瓶中 | |
| C. | 向氯化铝溶液滴入过量的氨水制备氢氧化铝 | |
| D. | 溴化银保存在无色玻璃瓶中 |
18.以下说法中正确的是( )
| A. | △S为负值的反应均不能自发进行 | |
| B. | △H<0的反应均是自发反应 | |
| C. | 高锰酸钾加热分解是一个熵减小的过程 | |
| D. | 冰在室温下自动熔化成水,是熵增的重要结果 |
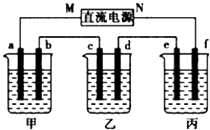 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g500%的NaOH溶液、足量的CuSO4溶液和l00g10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g500%的NaOH溶液、足量的CuSO4溶液和l00g10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
 如图所示,实验室用NH4Cl和Ca(OH)2制取NH3.试回答下列问题:
如图所示,实验室用NH4Cl和Ca(OH)2制取NH3.试回答下列问题: