题目内容
下列说法正确的是( )
| A、含有相同氧原子数的SO2和CO的质量相等 |
| B、等物质的量浓度的NaOH溶液与氨水中的c(OH-)相等 |
| C、乙酸分子与甲酸甲酯分子中的共价健数相等 |
| D、等温等压下,3mol C2H2(g)和1mol C6H6(g)的密度相等 |
考点:物质的量的相关计算,物质的量浓度,物质结构中的化学键数目计算
专题:计算题
分析:A.含有相同氧原子数的SO2和CO的物质的量之比为1:2,再根据m=nM判断;
B.一水合氨水弱电解质;
C.乙酸分子与甲酸甲酯分子核外同分异构体,含有的共价健数相等;
D.同温同压下,气体的密度之比等于其相对分子质量之比.
B.一水合氨水弱电解质;
C.乙酸分子与甲酸甲酯分子核外同分异构体,含有的共价健数相等;
D.同温同压下,气体的密度之比等于其相对分子质量之比.
解答:
解:A.含有相同氧原子数的SO2和CO的物质的量之比为1:2,二者质量之比=1mol×64g/mol:2mol×28g/mol=8:7,故A错误;
B.氢氧化钠完全电离,一水合氨水弱电解质,不能完全电离,二者浓度相同,溶液中c(OH-)不相等,故B错误;
C.乙酸结构简式为CH3COOH,甲酸甲酯结构简式为HCOOCH3,含有的共价健数相等,故C正确;
D.同温同压下,气体的密度之比等于其相对分子质量之比,故C2H2(g)与C6H6(g)的密度不相等,故D错误,
故选C.
B.氢氧化钠完全电离,一水合氨水弱电解质,不能完全电离,二者浓度相同,溶液中c(OH-)不相等,故B错误;
C.乙酸结构简式为CH3COOH,甲酸甲酯结构简式为HCOOCH3,含有的共价健数相等,故C正确;
D.同温同压下,气体的密度之比等于其相对分子质量之比,故C2H2(g)与C6H6(g)的密度不相等,故D错误,
故选C.
点评:本题考查物质的量有关计算,难度不大,D选项中注意根据PV=nRT理解阿伏伽德罗定律及其推论.

练习册系列答案
相关题目
浓硫酸不可以用来干燥的物质( )
| A、N2 |
| B、NH3 |
| C、SO2 |
| D、HCl |
用丙醛(CH3CH2CHO)制取聚丙烯的过程中发生的反应类型为( )
①取代反应②消去反应③加聚反应④氧化反应⑤还原反应.
①取代反应②消去反应③加聚反应④氧化反应⑤还原反应.
| A、①②③ | B、④②③ |
| C、⑤②④ | D、⑤②③ |
下列说法中正确的是( )
| A、把100mL3mol/L的硫酸与100mLH2O混合,硫酸的物质的量浓度变为1.5mol/L |
| B、用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2 |
| C、用CO2鉴别NaAlO2溶液和CH3COONa溶液 |
| D、用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
人体血液中的pH保持在7.35~7.45,适量的CO2可维持这个pH变化范围,可用下面化学方程式表示:H2O+CO2
H2CO3
H++HCO
,人呼出的气体中CO2的体积分数约为5%.下列说法中正确的是( )
| 肺 |
| 血液 |
- 3 |
| A、太快且太深的呼吸可导致酸中毒(pH过低) |
| B、太快且太深的呼吸可导致碱中毒(pH过高) |
| C、太慢且太浅的呼吸可导致碱中毒(pH过高) |
| D、呼吸快慢或深浅不会导致酸或碱中毒 |
下列分子中所有原子不可能同时存在同一平面上的是( )
A、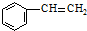 |
| B、CH2=CH2 |
| C、CH≡CCH3 |
| D、CH≡CH |
下列说法正确的是( )
| A、原电池是将电能转化为化学能的一种装置 |
| B、用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH |
| C、在原电池的负极和电解池的阴极上都发生失电子的氧化反应 |
| D、.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |