题目内容
(1)将适量的蔗糖放入一烧杯中,滴加几滴水后再加入一定量的浓硫酸并搅拌半分钟,此时可观察到蔗糖变黑,体积膨胀,并产生刺激性气味的气体,生成的黑色物质是 (填化学式),刺激性气味的气体主要成分是 (填化学式),该实验表明浓硫酸具有 性和 性.
(2)“绿色化学”要求综合考虑经济、技术、环保等方面来设计化学反应路线.若以铜为原料制取硫酸铜,请你设计复合“绿色化学”思想的反应路线(用化学方程式表示) .
(3)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消毒剂,工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,写出相应化学反应方程式,并用双线桥法标出电子转移方向和数目 ,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白,杀菌作用的次氯酸,化学反应方程式为 .
(4)工业上制备玻璃和水泥及工业上炼铁的共同原料是 (写名称).
(2)“绿色化学”要求综合考虑经济、技术、环保等方面来设计化学反应路线.若以铜为原料制取硫酸铜,请你设计复合“绿色化学”思想的反应路线(用化学方程式表示)
(3)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消毒剂,工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,写出相应化学反应方程式,并用双线桥法标出电子转移方向和数目
(4)工业上制备玻璃和水泥及工业上炼铁的共同原料是
考点:浓硫酸的性质,绿色化学,氯、溴、碘及其化合物的综合应用,含硅矿物及材料的应用
专题:元素及其化合物,化学应用
分析:(1)浓硫酸具有脱水性,将蔗糖脱水变成黑色的C;浓硫酸氧化C,同时被还原生成具有刺激性气味的二氧化硫;浓硫酸的脱水性和强氧化性;
(2)以铜为原料制取硫酸铜,符合“绿色化学”思想的反应,应先生成氧化铜,氧化铜与硫酸反应生成硫酸铜;
(3)氯气和石灰乳反应生成氯化钙和次氯酸钙;因碳酸酸性比次氯酸钙,则二氧化碳与漂白粉溶液反应生成次氯酸和碳酸钙沉淀;
(4)水泥的原料是粘土和石灰石,玻璃的原料是纯碱、石灰石和石英,所以原料中均有石灰石即碳酸钙,据此分析解答.
(2)以铜为原料制取硫酸铜,符合“绿色化学”思想的反应,应先生成氧化铜,氧化铜与硫酸反应生成硫酸铜;
(3)氯气和石灰乳反应生成氯化钙和次氯酸钙;因碳酸酸性比次氯酸钙,则二氧化碳与漂白粉溶液反应生成次氯酸和碳酸钙沉淀;
(4)水泥的原料是粘土和石灰石,玻璃的原料是纯碱、石灰石和石英,所以原料中均有石灰石即碳酸钙,据此分析解答.
解答:
解:(1)生成的黑色物质是浓硫酸将蔗糖脱水生成的C;
生成的具有刺激性气味的气体是二氧化硫,反应的化学方程式是:2H2SO4(浓)+C
CO2↑+2SO2↑+2H2O;
蔗糖逐渐变黑表现了浓硫酸的脱水性,放出有刺激性气味的气体说明浓硫酸具有强氧化性,
故答案为:C;SO2;脱水;强氧化;
(2)以铜为原料制取硫酸铜,符合“绿色化学”思想的反应,应先生成氧化铜,氧化铜与硫酸反应生成硫酸铜,反应的方程式为2Cu+O2
2CuO、CuO+H2SO4═CuSO4+H2O,
故答案为:2Cu+O2
2CuO、CuO+H2SO4═CuSO4+H2O;
(3)氯气和石灰乳反应生成氯化钙和次氯酸钙,反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,用双线桥标出电子转移的方向和数目为: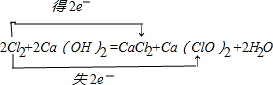 ,
,
因碳酸酸性比次氯酸钙,则二氧化碳与漂白粉溶液反应生成次氯酸和碳酸钙沉淀,反应的离子方程式为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
故答案为: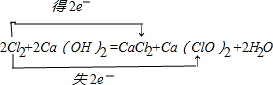 ;Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;
;Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;
(4)生产玻璃的原料是纯碱、石灰石和石英,高温下,碳酸钠、碳酸钙和二氧化硅反应分别生成硅酸钠、硅酸钙;
生产水泥以黏土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥;
所以在玻璃工业、水泥工业中都用到的原料是石灰石,
故答案为:石灰石.
生成的具有刺激性气味的气体是二氧化硫,反应的化学方程式是:2H2SO4(浓)+C
| ||
蔗糖逐渐变黑表现了浓硫酸的脱水性,放出有刺激性气味的气体说明浓硫酸具有强氧化性,
故答案为:C;SO2;脱水;强氧化;
(2)以铜为原料制取硫酸铜,符合“绿色化学”思想的反应,应先生成氧化铜,氧化铜与硫酸反应生成硫酸铜,反应的方程式为2Cu+O2
| ||
故答案为:2Cu+O2
| ||
(3)氯气和石灰乳反应生成氯化钙和次氯酸钙,反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,用双线桥标出电子转移的方向和数目为:
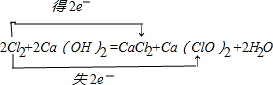 ,
,因碳酸酸性比次氯酸钙,则二氧化碳与漂白粉溶液反应生成次氯酸和碳酸钙沉淀,反应的离子方程式为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
故答案为:
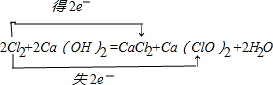 ;Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;
;Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;(4)生产玻璃的原料是纯碱、石灰石和石英,高温下,碳酸钠、碳酸钙和二氧化硅反应分别生成硅酸钠、硅酸钙;
生产水泥以黏土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥;
所以在玻璃工业、水泥工业中都用到的原料是石灰石,
故答案为:石灰石.
点评:本题考查浓硫酸的性质、物质制备实验方案的设计、漂白粉的组成及性质等知识,题目难度中等,试题侧重于学生的分析能力和元素化合物知识的综合运用的考查,注意浓硫酸的脱水性、漂白粉的组成及性质,把握绿色化学的要求,能够用双线桥法分析氧化还原反应.

练习册系列答案
相关题目
在298K下,铅室法生产硫酸存在如下三个平衡:下列有关说法正确的是( )
①SO2(g)+NO2(g)?SO3(g)+NO(g)△H1=-10.0kJ?mol-1
②2NO(g)+O2(g)?2NO2(g)△H2=-27.3kJ?mol-1
③2SO2(g)+O2(g)?2SO3(g)△H3.
①SO2(g)+NO2(g)?SO3(g)+NO(g)△H1=-10.0kJ?mol-1
②2NO(g)+O2(g)?2NO2(g)△H2=-27.3kJ?mol-1
③2SO2(g)+O2(g)?2SO3(g)△H3.
| A、298K,反应③的△H3═+47.3 kJ?mol-1 |
| B、平衡时,其他条件不变,升高温度,反应①中正反应速率加快 |
| C、平衡时,其他条件不变,增大NO2浓度可增大反应③中SO2转化率 |
| D、反应③中,每有1mol O=O键断裂,同时生成2molSO3,则该反应达平衡状态 |
下列物质的熔点高低顺序正确的是( )
| A、金刚石>碳化硅>晶体硅 |
| B、氧化铝>氯化钾>氯化钠 |
| C、H2O>NH3>PH3>AsH3 |
| D、SiC>生铁>纯铁>Mg |