题目内容
“盐荒”谣言:加碘食盐能预防放射性碘辐射.碘盐中常添加碘酸钾(KIO3),下列性质可以证明碘酸钾所属晶体类型的是( )
| A、具有较高的熔点 |
| B、熔融状态能导电 |
| C、水溶液能导电 |
| D、常温下能溶于水 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A、熔沸点:原子晶体>离子晶体>分子晶体,金属晶体熔点差异较大;
B、离子晶体都是电解质,某些分子晶体是电解质;
C、离子晶体都是电解质,某些分子晶体是电解质、非电解质,溶于水可以导电;
D、常温下是否溶于水与晶体类型无关.
B、离子晶体都是电解质,某些分子晶体是电解质;
C、离子晶体都是电解质,某些分子晶体是电解质、非电解质,溶于水可以导电;
D、常温下是否溶于水与晶体类型无关.
解答:
解:A、熔沸点:原子晶体>离子晶体>分子晶体,金属晶体熔点差异较大,具有较高的熔点,可以证明氯酸钾为离子晶体,故A正确;
B、离子晶体都是电解质,某些分子晶体是电解质,在熔融状态下可以导电,故B错误;
C、离子晶体都是电解质,某些分子晶体是电解质、非电解质,溶于水可以导电,故C错误;
D、常温下是否溶于水与晶体类型无关,离子晶体、分子晶体中都有可溶于水的物质,故D错误;
故选A.
B、离子晶体都是电解质,某些分子晶体是电解质,在熔融状态下可以导电,故B错误;
C、离子晶体都是电解质,某些分子晶体是电解质、非电解质,溶于水可以导电,故C错误;
D、常温下是否溶于水与晶体类型无关,离子晶体、分子晶体中都有可溶于水的物质,故D错误;
故选A.
点评:本题考查了从物理性质判断晶体类型的方法,题目难度一般,注意晶体与电解质是完全无关的两个概念.

练习册系列答案
相关题目
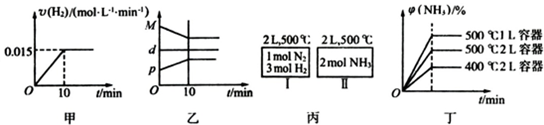
合成氨的热化学方程式为N2(g)+3H2(g)2NH3(g)△H=-92.4kJ?mol-1.现将1molN2(g)、3molH2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,NH3的体积分为?,下列说法中正确的是
 ( )
( )
 ( )
( )| A、若达到平衡时,测得体系放出9.24kJ热量,则H2反应速率变化曲线如图甲所示 |
| B、反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p,三者关系如图乙 |
| C、如图丙所示,容器I和II达到平衡时所需要的时间可能不同 |
| D、若起始加入物料为1 mol N2,3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图丁所示 |
以下5种有机物的分子式都是C4H10O:
①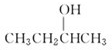 ②
②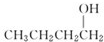 ③
③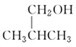 ④
④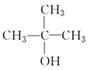 ⑤CH3CH2OCH2CH3.
⑤CH3CH2OCH2CH3.
其中能被氧化为含相同碳原子数的醛的是( )
①
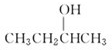 ②
②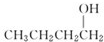 ③
③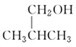 ④
④ ⑤CH3CH2OCH2CH3.
⑤CH3CH2OCH2CH3.其中能被氧化为含相同碳原子数的醛的是( )
| A、①② | B、只有② |
| C、②③ | D、③④⑤ |
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:

关于咖啡鞣酸的下列叙述正确的是( )

关于咖啡鞣酸的下列叙述正确的是( )
| A、分子式为C16H13O9 |
| B、1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应 |
| C、能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键 |
| D、与浓溴水能发生两种类型的反应 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
| B、标准状况下,2.24 L Cl2与过量NaOH溶液反应,转移的电子总数为0.2NA |
| C、1 mol/L的NaOH溶液中含Na+数目为NA |
| D、标准状况下,11.2 L CCl4中的C-Cl键数目为2NA |
下列有关化学反应速率的描述中正确的是( )
| A、在任何化学反应中,只要提高反应温度,就可提高反应速率 |
| B、在任何化学反应中,只要增大某一反应物的用量,就会增大反应速率 |
| C、在任何化学反应中,增大压强时,都会使反应速率增大 |
| D、在任何化学反应中,只要缩小容器的体积,都会使反应速率增大 |
某气态烃10mL与50mL氧气在一定条件下作用,刚好耗尽反应物,生成水蒸气40mL、一氧化碳和二氧化碳各20mL(各体积都是在同温同压下测得).该气态烃为( )
| A、C3H8 |
| B、C4H6 |
| C、C3H6 |
| D、C4H8 |
2011年3月日本福岛大地震引起的核泄漏污染物中含有
I等放射性同位素,该同位素原子核内中子数和核外电子数之差为( )
131 53 |
| A、25 | B、78 |
| C、103 | D、184 |

