题目内容
20.三氧化二锰(Mn2O3)在现代工业上应用广泛,在锂离子电池的制备中有重要的作用.用软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)制备高纯度Mn2O3的工艺流程如图所示.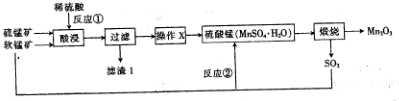
(1)反应①中会生成一种非金属单质,则该非金属单质是S,该反应的还原剂是MnS.(填化学式)
(2)操作X为蒸发浓缩、冷却结晶、过滤、洗涤烘干.在洗涤操作中,常用酒精洗涤MnSO4•H2O晶体,主要目的是MnSO4•H2O在酒精中溶解度小,可减小MnSO4•H2O的损失;
(3)Mn2O3与MnO2类似,加热时也能与浓盐酸反应放出Cl2,该反应的离子方程式为Mn2O3+6H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$2Mn2++Cl2↑+3H2O.
分析 软锰矿和硫锰矿加入稀硫酸充分浸泡,发生MnO2+MnS+4H+=2Mn2++S↓+2H2O,得到滤渣1含有S,滤液含有锰离子,将滤液蒸发浓缩、冷却结晶、过滤、洗涤烘干得到硫酸锰晶体,煅烧可得到Mn2O3,以此解答该题.
解答 解:软锰矿和硫锰矿加入稀硫酸充分浸泡,发生MnO2+MnS+4H+=2Mn2++S↓+2H2O,得到滤渣1含有S,滤液含有锰离子,将滤液蒸发浓缩、冷却结晶、过滤、洗涤烘干得到硫酸锰晶体,煅烧可得到Mn2O3,
(1)反应①中是利用稀硫酸溶解MnO2和MnS的混合物得到MnSO4,反应中+4价Mn发生还原反应,同时S2-发生氧化反应生成S,发生反应的离子方程式为MnO2+MnS+4H+=2Mn2++S↓+2H2O,故所得非金属单质为S,反应中的还原剂是MnS,故答案为:S;MnS;
(2)操作X的目的是从MnSO4溶液里获得MnSO4•H2O晶体,具体操作是蒸发浓缩、冷却结晶、过滤、洗涤烘干.因MnSO4•H2O在酒精中溶解度小,在洗涤操作中,常用酒精洗涤MnSO4•H2O晶体,可减小MnSO4•H2O的损失,故答案为:冷却结晶;MnSO4•H2O在酒精中溶解度小,可减小MnSO4•H2O的损失;
(3)加热时Mn2O3与浓盐酸反应放出Cl2的同时生成MnCl2和H2O,该反应的离子方程式为Mn2O3+6H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$2Mn2++Cl2↑+3H2O,
故答案为:Mn2O3+6H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$2Mn2++Cl2↑+3H2O.
点评 本题考查物质制备实验方案设计,为高频考点,侧重考查学生获取信息利用信息解答问题能力及对基本知识的灵活运用,涉及方程式和离子方程式的书写、氧化还原反应、物质分离和提纯等知识点,明确反应原理、物质性质是解本题关键,题目难度中等.

| A. | 硝基、羟基、氯原子、苯环、甲基都是官能团 | |
| B. | 邻二甲苯不存在同分异构体,说明苯分子中所有的碳碳键都是完全相同的 | |
| C. | 乙烯、苯分子中所有原子共平面 | |
| D. | CH2Cl2有两种同分异构体 |
| A. | CH2=CH2+Br2→CH2BrCH2Br | B. | 2CH3CH3+Cl2$\stackrel{光照}{→}$2CH3CH2Cl+H2 | ||
| C. | CH3CH2OH+Na→CH3CH2ONa+H2↑ | D. | 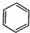 +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$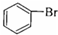 +HBr +HBr |
| A. | 1.6g臭氧中含有的氧原子数为0.1NA | |
| B. | 18gD2O中含有的质子数为10NA | |
| C. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| D. | 标准状况下,11.2L己烷含有的分子数为0.5NA |
(1)Si位于元素周期表第三周期IV族;3He原子核内的中子数为1;
(2)用“>”或“<”填空:
| 离子半径 | 第一电力能 | 熔点 | 酸性 |
| O2->Na+ | Si<S | NaCl<NaF | HClO4>H2SO4 |
(4)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取.写出该反应的离子方程式2ClO2-+Cl2=2ClO2+2Cl-.
| A. | 在2 min内的反应速率用B表示为0.3 mol/(L•min) | |
| B. | 在2 min内用A表示反应速率是0.4 mol/(L•min) | |
| C. | 在2 min内用C表示反应速率是0.2 mol/(L•min) | |
| D. | 当V正(B)=3V逆(D)时,反应达到平衡 |
 研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.(1)CO可用于炼铁,已知:
Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1.
(2)分离高炉煤气得到的CO与空气可设计成燃料电池,若电解质为碱性.写出该燃料电池的负极反应式CO+4OH--2e-=CO32-+2H2O.
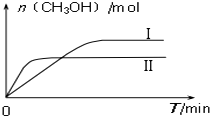
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);测得CH3OH的物质的量随时间的变化图:
①由图判断该反应△H< 0,曲线 I、II对应的平衡常数KI>KII(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
③一定温度下,此反应在恒容密闭容器中进行,能判断该反应达到化学平衡状态的依据是a b.
a.容器中压强不变 b.H2的体积分数不变 c.c(H2)=3c(CH3OH)
d.容器中密度不变 e.2个C=O断裂的同时有3个C-H形成
(4)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g).二甲醚可用作直接燃料电池,1mol二甲醚分子经过电化学氧化,可以产生12NA个电子的电量;根据化学反应原理,分析增加压强对制备二甲醚反应的影响该反应分子数减少,压强增加使平衡右移,CH3OCH3产率增加;压强增加使CO和H2浓度增加,反应速率增大.