题目内容
18.下列说法正确的是( )| A. | 除去甲烷气体中的乙烯可以将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶 | |
| B. | 苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环结构 | |
| C. | 乙酸和乙醇在浓硫酸作用下可以反应,该反应属于加成反应 | |
| D. | 乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 |
分析 A.乙烯被高锰酸钾氧化生成二氧化碳;
B.苯中不存在碳碳双键;
C.酯化反应为取代反应;
D.乙烯中碳碳双键,苯中的化学键介于单、双键之间的特殊化学键.
解答 解:A.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,不能除杂,应选溴水、洗气,故A错误;
B.苯中不存在碳碳双键,苯的二氯代物有邻、间、对3种,故B错误;
C.乙酸和乙醇在浓硫酸作用下发生的酯化反应为取代反应,故C错误;
D.乙烯中碳碳双键,苯中的化学键介于单、双键之间的特殊化学键,乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,侧重于学生的分析能力、应用能力的考查,把握官能团与性质的关系、有机反应为解答的关键,题目难度不大.

练习册系列答案
相关题目
8.反应CO2(g)+2NH3(g)?CO(NH2)2(s)+H2O(g)△H<0,达到平衡时,下列说法正确的是( )
| A. | 加入催化剂,平衡常数不变 | |
| B. | 减小容器体积,正反应速率增大、逆反应速率减小 | |
| C. | 增大CO(NH2)2的量,CO2的转化率减小 | |
| D. | 降低温度,平衡向逆反应方向移动 |
9.下列说法错误的是( )
| A. | I的原子半径大于Br,HI比HBr的热稳定性强 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | 锂所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3 | |
| D. | 与水或者酸反应的剧烈程度:K>Na>Mg |
6.恒温下,容积为2L的定容密闭容器中,充入3molA、y mol B,发生反应:3A(g)+2B(g)?2C(g)+xD(g).2min后达到平衡,测得从反应开始到平衡时C的速率为0.3mol•L-1•min-1.下列推断的结论正确的是( )
| A. | y≥1.2 | |
| B. | 增大反应体系的压强,反应速率不一定增大 | |
| C. | v正(A)>v逆(C),不可能为平衡状态 | |
| D. | 混合气体的密度不再变化,一定为平衡状态 |
13.戊酸(C5H10O2)与丁醇(C4H10O)存一定条件下反应,生成酯有( )
| A. | 12种 | B. | 16种 | C. | 20种 | D. | 40种 |
3.分子式为C5H12的烃有多种,其中一氯代物最多的烃的分子中含有的甲基数为( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
10.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),如图:下列判断错误的是( )
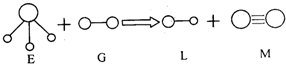
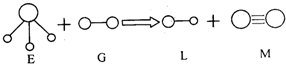
| A. | G是最活泼的非金属单质 | B. | L能使紫色石蕊试液变红色 | ||
| C. | E能使紫色石蕊试液变蓝色 | D. | M是化学性质很活泼的单质 |
8.下列元素属于第三周期的是( )
| A. | 氢 | B. | 氧 | C. | 氯 | D. | 碘 |