题目内容
下列离子方程式不正确的是( )
| A、将一小粒金属钠放入水中:2Na+2H2O═2Na++2OH-+H2↑ |
| B、将氯气通入氢氧化钠溶液中:Cl2+2OH-═C1-+C1O-+H2O |
| C、向CuSO4溶液中加入适量Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
| D、向稀硝酸中加人铜片:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.Na与水反应生成NaOH和氢气,NaOH为强电解质;
B.反应生成氯化钠、次氯酸钠、水;
C.漏写溶液中铜离子和氢氧根离子反应生成的沉淀;
D.离子方程式遵循电荷守恒.
B.反应生成氯化钠、次氯酸钠、水;
C.漏写溶液中铜离子和氢氧根离子反应生成的沉淀;
D.离子方程式遵循电荷守恒.
解答:
解:A.Na与水反应生成NaOH和氢气,NaOH为强电解质,反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故A正确;
B.氯气通入氢氧化钠溶液中的离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故B正确;
C.向CuSO4溶液中加入适量Ba(OH)2溶液:Cu2++2OH-+Ba2++SO42-═BaSO4↓+Cu(OH)2↓,故C错误;
D.铜与稀硝酸反应反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故D正确.
故选C.
B.氯气通入氢氧化钠溶液中的离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故B正确;
C.向CuSO4溶液中加入适量Ba(OH)2溶液:Cu2++2OH-+Ba2++SO42-═BaSO4↓+Cu(OH)2↓,故C错误;
D.铜与稀硝酸反应反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故D正确.
故选C.
点评:本题考查离子方程式的书写,题目难度不大,注意从电荷守恒、粒子符号、反应是否符合实际等角度思考.

练习册系列答案
相关题目
如图是一套电化学装置,对其有关说法错误的是( )

| A、装置A是原电池,装置B是电解池 |
| B、反应一段时间后,装置B中溶液PH增大 |
| C、a口若消耗1mol CH4,d口可产生4mol气体 |
| D、a口通入C2H6时的电极反应为 C2H6-14e-+18OH-═2CO32-+12H2O |
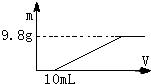 过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5mol?L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为( )
过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5mol?L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为( )| A、0.05mol |
| B、0.1mol |
| C、0.2mol |
| D、0.25mol |
下列各组内物质间的反应,可以用同一个离子方程式表示的是( )
| A、H2SO4和NaOH;HNO3和Ba(OH)2 |
| B、H2SO4和Ba(OH)2;BaCl2和Na2SO4 |
| C、HCl和NH3?H2O;CH3COOH和NaOH |
| D、H2SO4和NaOH;H2SO4和Cu(OH)2 |
下列离子方程式书写错误的是( )
| A、向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42-+H++Ba2++OH-=BaSO4↓+H2O |
| B、少量小苏打溶液滴入Ba(OH)2溶液中:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| C、碳酸氢根离子发生电离:HCO3-+H2O?H3O++CO32- |
| D、将1mol?L-1 NaAlO2溶液和1.5mol?L-1 HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |


