题目内容
13.下列不是铁的氧化物的是( )| A. | Fe3O4 | B. | Fe2O3 | C. | FeCl2 | D. | FeO |
分析 氧化物即由两种元素构成,其中一种为氧元素的化合物.而铁的氧化物,即由两种元素构成,其中元素为氧元素,而另一种元素为铁元素的化合物,据此分析.
解答 解:氧化物即由两种元素构成,其中一种为氧元素的化合物.而铁的氧化物,即由两种元素构成,其中元素为氧元素,而另一种元素为铁元素的化合物,故Fe3O4、Fe2O3、FeO均为铁的氧化物,而FeCl2不是铁的氧化物,只属于铁的化合物,故选C.
点评 本题较简单,主要从概念上抓住判断的关键点,两个关键缺一不可,要同时具备.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
3.将浓度为0.1mol•L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A. | [H+] | B. | Ka(HF) | C. | $\frac{[{F}^{-}]}{[{H}^{+}]}$ | D. | $\frac{[{H}^{+}]}{[HF]}$ |
4.下列说法正确的是( )
| A. | 分子式为C7H8O,且含苯环的有机化合物有4种 | |
| B. | 乙醇能使酸性高锰酸钾溶液褪色 | |
| C. | 向无水乙醇中加入浓H2SO4,加热至170℃,产生的使酸性KMnO4溶液褪色的气体只是乙烯 | |
| D. | 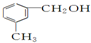 遇FeCl3溶液可显紫色 遇FeCl3溶液可显紫色 |
1.下列溶液中有关粒子的物质的量浓度关系正确的是( )
| A. | 氯水中:2c(Cl2)=c(ClO-)+c(Cl-)+c(HClO) | |
| B. | 25℃时,pH=12的NaOH溶液与pH=12的氨水:c (Na+)=c(NH4+ ) | |
| C. | pH=4的0.1 mol•L-1的NaHA溶液中:c(HA-)>c(H+)>c(H2A)>c(A2-) | |
| D. | 在K2CO3溶液中:c(CO32-)+c(OH-)=c(HCO3-)+c( H+) |
8.某溶液含有K+、Fe3+、SO42-,CO32-、I-中的几种.取样,滴加KSCN溶液后显血红色.不正确的是( )
| A. | 一定存在的离子为Fe3+、SO42- | |
| B. | 一定不存在的离子为CO32-、I- | |
| C. | 不能确定的离子为K+、SO42- | |
| D. | 确定是否含有K+离子需要经过焰色反应 |
18.下列各组离子因发生氧化还原反应而不能大量共存的是( )
| A. | H+、Fe2+、MnO4-、SO42- | B. | Ca2+、H+、SO42-、HCO3- | ||
| C. | Na+、Cu2+、Cl-、S2- | D. | Fe3+、K+、SCN-、Cl- |
5.下列说法正确的是( )
| A. | 物质发生化学变化都伴随着能量变化 | |
| B. | 任何反应中的能量变化都表现为热量变化 | |
| C. | 伴有能量变化的物质变化都是化学变化 | |
| D. | 所有化学反应都可以设计成原电池 |
2.(1)BrO3-+Cl2═Br2+2ClO3-(2)5Cl2+I2+6H2O═2HIO3+10HCl
(3)ClO3-+5Cl-+6H+═3Cl2+3H2O,由上述反应,判断氧化能力强弱,正确的是( )
(3)ClO3-+5Cl-+6H+═3Cl2+3H2O,由上述反应,判断氧化能力强弱,正确的是( )
| A. | ClO3->BrO3->IO3->Cl2 | B. | BrO3->Cl2>IO3->ClO3- | ||
| C. | BrO3->ClO3->Cl2>IO3- | D. | Cl2>BrO3->ClO3->IO3- |
3.用聚光手电筒照射下列分散系,不能观察到丁达尔效应的是( )
| A. | KOH溶液 | B. | Fe(OH)3胶体 | C. | 雾 | D. | 鸡蛋清水溶液 |