题目内容
4.下面对SO2和CO2的描述正确的是( )| A. | SO2为原子晶体,CO2为分子晶体 | |
| B. | 中心原子采取的杂化方式:SO2为sp2杂化,CO2为sp杂化 | |
| C. | 都是直线形结构 | |
| D. | S原子和C原子上都没有孤电子对 |
分析 A、SO2、CO2都是分子晶体;
B、SO2中S原子形成2个σ键,孤电子对个数=$\frac{1}{2}$×(6-2×2)=1,价层电子对数为3,为sp2杂化;而二氧化碳分子中价层电子对个数=σ键个数+孤电子对个数=2+$\frac{1}{2}$(4-2×2)=2,采取sp杂化方式;
C、SO2为折线型,而二氧化碳是直线型;
D、SO2中S原子上有孤电子对.
解答 解:A、SO2、CO2都是分子晶体,故A错误;
B、SO2中S原子形成2个σ键,孤电子对个数=$\frac{1}{2}$×(6-2×2)=1,价层电子对数为3,为sp2杂化;而二氧化碳分子中价层电子对个数=σ键个数+孤电子对个数=2+$\frac{1}{2}$(4-2×2)=2,采取sp杂化方式,所以中心原子采取的杂化方式:SO2为sp2杂化,CO2为sp杂化,故B正确;
C、SO2为折线型,而二氧化碳是直线型,故C错误;
D、SO2中S原子上有孤电子对,二氧化碳无孤电子对,故D错误;
故选B.
点评 本题考查了原子杂化类型的判断、晶体类型的判断,题目难度中等,原子杂化类型的判断是高考的热点,根据“杂化轨道数=σ键数+孤对电子对数”解答,比较容易.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.经检测某工厂的酸性废水中所含离子及其浓度如下表所示:
(1)c(H+)=0.01mol/L.
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4•7H2O).
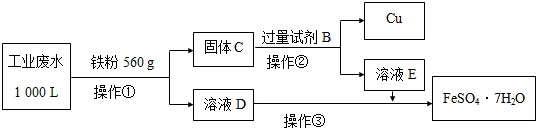
①工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+═Fe2++Cu、Fe+2Fe3+═3Fe2+、Fe+2H+═Fe2++H2↑.
②试剂B是H2SO4.
③操作③是蒸发浓缩、冷却结晶、过滤,最后用少量冷水洗涤晶体,在低温下干燥.
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是取少量D中溶液于试管中,滴加1滴KSCN溶液,不出现红色,说明废水中Fe3+除尽.
⑤获得的FeSO4•7H2O需密闭保存,原因是FeSO4有还原性,易被氧化(或FeSO4•7H2O失去结晶水).
⑥上述1000L废水经处理,可获得 FeSO4•7H2O的物质的量是12mol.
| 离子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
| 浓度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4•7H2O).

①工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+═Fe2++Cu、Fe+2Fe3+═3Fe2+、Fe+2H+═Fe2++H2↑.
②试剂B是H2SO4.
③操作③是蒸发浓缩、冷却结晶、过滤,最后用少量冷水洗涤晶体,在低温下干燥.
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是取少量D中溶液于试管中,滴加1滴KSCN溶液,不出现红色,说明废水中Fe3+除尽.
⑤获得的FeSO4•7H2O需密闭保存,原因是FeSO4有还原性,易被氧化(或FeSO4•7H2O失去结晶水).
⑥上述1000L废水经处理,可获得 FeSO4•7H2O的物质的量是12mol.
9.下列实验操作正确的是( )
| A. | 过滤时用玻璃棒搅拌漏斗里的液体 | |
| B. | 加热后的蒸发皿用坩埚钳夹取 | |
| C. | 用自来水制蒸馏水实验中,将温度计水银球插到蒸烧瓶自来水中 | |
| D. | 从碘水中提取单质碘时,可用无水乙醇代替CCl4 |
16.铝、铁的混合物溶于足量的盐酸中,再加入过量的NaOH溶液,在空气中静置,当红褐色沉淀不再增加,将沉淀滤出并充分灼烧,得到的固体残留物恰好跟原混合物的质量相等,则此合金中铝的质量分数为( )
| A. | 22.2% | B. | 30.0% | C. | 75.7% | D. | 80.6% |
13.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18g冰中最多含有氢键的数目为4NA | |
| B. | 0.1L3mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3NA | |
| C. | 7.8gNa2O2中阴、阳离子总数为0.4NA | |
| D. | 4.5gSiO2晶体中含有的硅氧键数目为0.3NA |
14.下列电离方程式书写正确的是( )
| A. | Na3PO4═3Na++P5++4O2- | B. | H2SO4═H++SO42- | ||
| C. | NH3•H2O?NH4++O2-+H+ | D. | NH4NO3═NH4++NO3- |
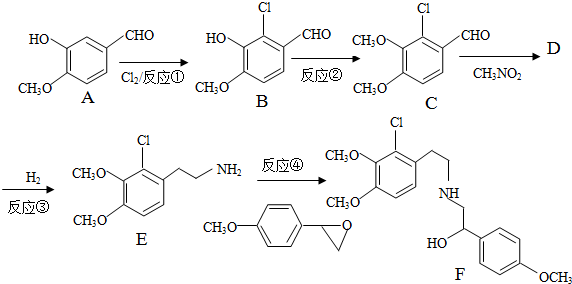
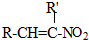 +H2O
+H2O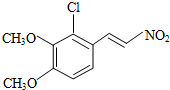 ,反应③中1摩尔D需要4摩尔H2才能转化为E
,反应③中1摩尔D需要4摩尔H2才能转化为E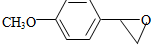 很多种同分异构体,请写出符合下列条件的一种同分异构体的结构简式
很多种同分异构体,请写出符合下列条件的一种同分异构体的结构简式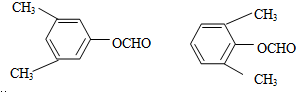 .
.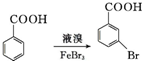 .写出以
.写出以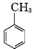 为原料制备
为原料制备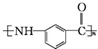 的合成路线流程图(无机试剂任选).(合成路线常用表示方法为:A$→_{反应试剂}^{反应试剂}$B …$→_{反应试剂}^{反应试剂}$目标产物)
的合成路线流程图(无机试剂任选).(合成路线常用表示方法为:A$→_{反应试剂}^{反应试剂}$B …$→_{反应试剂}^{反应试剂}$目标产物)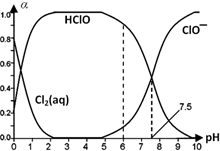 Cl2及其化合物在生产、生活中有广泛用途,回答下列问题.
Cl2及其化合物在生产、生活中有广泛用途,回答下列问题. HClO+H++Cl-或Cl2(aq)+H2O
HClO+H++Cl-或Cl2(aq)+H2O HClO+HCl、HClO
HClO+HCl、HClO H++ClO-.
H++ClO-.