题目内容
17.原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物.(1)写出Y2O2的电子式:
 .
.(2)用电子式表示Y2O的形成过程
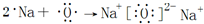 .
.(3)X、Z、W三种元素的最高价氧化物对应的水化物中,溶液酸性最强的是HClO4(填化学式).
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是NH3(填化学式).
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式NCl3+3H2O═3HClO+NH3.
分析 原子序数由小到大排列的四种短周期元素X、Y、Z、W,Y与氧元素可组成Y2O和Y2O2离子化合物,则Y为钠元素,X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物,X原子序数都小于钠,所以X为氮元素,Z、W原子序数都大于钠,Z为硫元素,W为氯元素,以此来答题.
解答 解:原子序数由小到大排列的四种短周期元素X、Y、Z、W,Y与氧元素可组成Y2O和Y2O2离子化合物,则Y为钠元素,X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物,X原子序数都小于钠,所以X为氮元素,Z、W原子序数都大于钠,Z为硫元素,W为氯元素,
(1)过氧化钠的电子式为 ,故答案为:
,故答案为: ;
;
(2)用电子式表示Na2O的形成过程为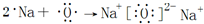 ,故答案为:
,故答案为: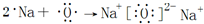 ;
;
(3)非金属性越强,元素的最高价氧化物对应的水化物的酸性越强,在氮、硫、氯中氯元素的非金属性最强,所以酸性最强的是HClO4,
故答案为:HClO4;
(4)NH3与H2S和HCl都能反应,生成对应的铵盐,故答案为:NH3;
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,则该化合物为NCl3,遇水可生成一种具有漂白性的化合物为次氯酸和一种刺激性气味的气体则为氨气,反应的化学方程式为NCl3+3H2O═3HClO+NH3,
故答案为:NCl3+3H2O═3HClO+NH3.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素化合物知识推断元素为解答的关键,侧重分析与推断能力、应用能力的考查,题目难度不大.

练习册系列答案
相关题目
7.下列化学用语正确的是( )
| A. | H2S的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | Mg2+的结构示意图: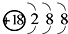 | |
| C. | Na2O的电子式:Na${\;}_{2}^{+}$[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2- | |
| D. | N2的电子式: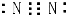 |
8.关于碱金属的叙述不正确的是( )
| A. | 熔点:Li>Na>K>Rb>Cs | |
| B. | 碱性:LiOH<NaOH<KOH<RbOH<CsOH | |
| C. | 与水反应的剧烈程度:Li<Na<K<Rb<Cs | |
| D. | 都能在空气中燃烧生成R2O(R表示碱金属) |
5.a、b、c、d是四种短周期元素.a、b、d同周期,c、d同主族.a的原子结构示意图为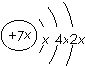 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为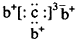 .下列比较中正确的是( )
.下列比较中正确的是( )
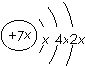 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为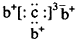 .下列比较中正确的是( )
.下列比较中正确的是( )| A. | 原子半径:a>c>d>b | B. | 非金属性 b>d>c | ||
| C. | 原子序数:d>a>c>b | D. | 最高价含氧酸的酸性c>d>a |
12.首次成功解释了氢原子光谱的科学家是( )
| A. | 道尔顿 | B. | 卢瑟福 | C. | 玻尔 | D. | 爱因斯坦 |
2.下列有关金属的说法中,正确的是( )
①钠着火可用水扑灭; ②铝在空气中不易被腐蚀,所以铝是不活泼金属; ③生铁在潮湿的空气中可发生吸氧腐蚀; ④人体缺钙会引起骨质疏松、缺铁会引起贫血; ⑤青铜、不锈钢、硬铝都是合金; ⑥Al和Fe在一定条件下能与某些氧化物反应.
①钠着火可用水扑灭; ②铝在空气中不易被腐蚀,所以铝是不活泼金属; ③生铁在潮湿的空气中可发生吸氧腐蚀; ④人体缺钙会引起骨质疏松、缺铁会引起贫血; ⑤青铜、不锈钢、硬铝都是合金; ⑥Al和Fe在一定条件下能与某些氧化物反应.
| A. | ①②⑤ | B. | ②③⑤ | C. | ③④⑤⑥ | D. | 全都正确 |
9.弱酸HCN溶液中存在着下列平衡:HCN?H++CN-,若要使平衡逆向移动,同时使c(H+)增大,应加入适量的下列物质是( )
| A. | 硫酸 | B. | NaOH固体 | C. | NaCN固体 | D. | 水 |
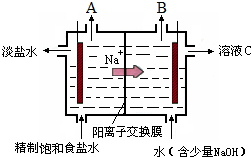 氯碱工业中电解饱和食盐水的原理示意图如图所示:
氯碱工业中电解饱和食盐水的原理示意图如图所示: