题目内容
实验测得某些食物的近似pH如表,下列说法正确的是( )
| 食物 | 泡菜 | 葡萄 | 番茄 | 苹果 | 牛奶 | 玉米粥 |
| pH | 3.4 | 4.2 | 4.4 | 3.1 | 6.5 | 7.8 |
| A、牛奶和玉米粥均属于碱性食物 |
| B、胃酸过多的人应少食泡菜 |
| C、番茄的酸性比苹果强 |
| D、用湿润的pH试纸蘸取葡萄汁测其pH |
考点:溶液pH的定义
专题:电离平衡与溶液的pH专题
分析:A.当溶液的pH大于7时,呈碱性;
B.胃酸内含有盐酸显强酸性,胃酸过多的病人要少食用酸性食品;
C.当溶液的pH小于7时,呈酸性,且随着pH的减小酸性增强;
D.测定溶液的pH值用玻璃棒蘸取待测液滴在干燥的pH试纸上.
B.胃酸内含有盐酸显强酸性,胃酸过多的病人要少食用酸性食品;
C.当溶液的pH小于7时,呈酸性,且随着pH的减小酸性增强;
D.测定溶液的pH值用玻璃棒蘸取待测液滴在干燥的pH试纸上.
解答:
解:A.牛奶的pH小于7,显酸性,玉米粥的pH大于7,显碱性,故A错误;
B.胃酸过多为盐酸过多,泡菜的pH小于7,显酸性,所以胃酸过多的人应少食泡菜,故B正确;
C.番茄的pH大于苹果的pH,所以番茄的酸性比苹果弱.故C错误;
D.用湿润的pH试纸蘸取葡萄汁测其pH,导致原溶液被稀释,应该用干燥的pH试纸,并且是把葡萄汁滴在pH试纸上测其pH,故D错误;
故选B.
B.胃酸过多为盐酸过多,泡菜的pH小于7,显酸性,所以胃酸过多的人应少食泡菜,故B正确;
C.番茄的pH大于苹果的pH,所以番茄的酸性比苹果弱.故C错误;
D.用湿润的pH试纸蘸取葡萄汁测其pH,导致原溶液被稀释,应该用干燥的pH试纸,并且是把葡萄汁滴在pH试纸上测其pH,故D错误;
故选B.
点评:本题主要考查食物的pH有关问题,解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列分离提纯方法不正确的是( )
| A、分离KNO3和氯化钠,常用结晶与重结晶 |
| B、提纯含有碘的食盐,常用升华法 |
| C、去除乙醇中的水分离常用蒸馏法 |
| D、苯和酸性高锰酸钾溶液可用分液法 |
下列事实不能用勒夏特列原理(平衡移动原理)解释的是( )
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④保存FeCl2溶液时向溶液中加入少量铁粉
⑤钠与氯化钾共融制备钾Na(L)+KCl(L)?K(g)+NaCl(L);
⑥二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深.
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④保存FeCl2溶液时向溶液中加入少量铁粉
⑤钠与氯化钾共融制备钾Na(L)+KCl(L)?K(g)+NaCl(L);
⑥二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深.
| A、①②③ | B、②④⑥ |
| C、③④⑤ | D、②⑤⑥ |
某无色溶液能与Al反应放出H2,下列离子可能在该溶液中大量共存的是( )
| A、K+、H+、NO3-、Fe2+ |
| B、Na+、SO42-、Mg2+、Cl- |
| C、Ba2+、K+、OH-、SO42- |
| D、Al3+、Mg2+、SiO32-、ClO- |
下列有关实验的原理、方法和结论都正确的是( )
| A、将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH变化大 |
| B、用CH3COOH溶液作导电性实验,灯光较暗,说明CH3COOH是弱电解质 |
| C、向滴有酚酞的Na2CO3溶液中逐滴加入Ba(NO3)2,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
| D、沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
有一分子式为C8H14N2O3的二肽,经水解后得到丙氨酸CH3CH(NH2)COOH和另一种氨基酸R,则R的分子式为( )
| A、C5H9NO |
| B、C5H9NO2 |
| C、C5H9NO3 |
| D、C5H9NO4 |
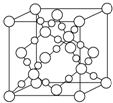 A、B、C、D、E、F是周期表中的前20号元素,原子序数逐渐增大.
A、B、C、D、E、F是周期表中的前20号元素,原子序数逐渐增大.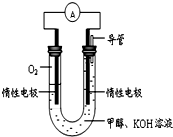 某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.