题目内容
30.一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。(1)原NaOH溶液的质量分数为
(2)所得溶液中Cl-的物质的量为 mol
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)= 。
(1)10.7% (2)0.25 (3)3︰2
解析:本题是有关氯气性质的计算题。由物质的量浓度与质量分数的互换公式
w(NaOH)=![]() ×100%=
×100%=![]() ×100%=10.7%
×100%=10.7%
Cl2+H2![]() 2HCl
2HCl
Cl2+2NaOH===NaCl+NaClO+H2O
HCl+NaOH===NaCl+H2O
n(Cl-)=n(Na+)-n(ClO-)=![]() ×3.00 mol·L-1-0.050 0 mol=0.25 mol。与NaOH反应Cl2的物质的量为0.050 mol。Cl2与H2反应生成HCl的物质的量为:n(HCl)=0.25 mol-0.05 mol=0.20 mol,所用氯气和参加反应的氢气的物质的量之比
×3.00 mol·L-1-0.050 0 mol=0.25 mol。与NaOH反应Cl2的物质的量为0.050 mol。Cl2与H2反应生成HCl的物质的量为:n(HCl)=0.25 mol-0.05 mol=0.20 mol,所用氯气和参加反应的氢气的物质的量之比
![]() =
=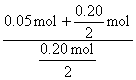 =
=![]()

练习册系列答案
相关题目