题目内容
1.过氧化钠淡黄色固体,与CO2反应,方程式2Na2O2+2CO2=2Na2CO3+O2.因此,过氧化钠可作为呼吸面具和潜水艇的氧气来源.分析 过氧化钠为淡黄色固体,与二氧化碳反应生成碳酸钠和氧气,可作供氧剂,以此来解答.
解答 解:过氧化钠为淡黄色固体,与CO2反应,方程式为2Na2O2+2CO2=2Na2CO3+O2,因此,过氧化钠可作为呼吸面具和潜水艇的氧气来源,
故答案为:淡黄;2Na2O2+2CO2=2Na2CO3+O2.
点评 本题考查钠的化合物,为高频考点,把握物质的性质、发生的反应、性质与用途为解答关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 向反应后的深蓝色溶液中加入乙醇,会有蓝色的CuSO4•5H2O晶体析出 | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| C. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的数目不变 | |
| D. | 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ |
12.某溶液中加入铝粉有氢气产生,该溶液中肯定可以大量共存的离子组是( )
| A. | Na+NO3-CO32- Cl- | B. | HCO3-Ba2+ Na+ K+ | ||
| C. | Cl- Na+ K+ SO42- | D. | K+Fe2+SO42- Cl- |
9.下列分子中,具有极性共价键的非极性分子的是( )
| A. | l2 | B. | NH3(三角锥型) | C. | CO2 | D. | SO2(键角120°) |
16.下列液体能漂白有色布条的是( )
| A. | 氨水 | B. | 氯水 | C. | 食盐水 | D. | 蒸馏水 |
6.A、B、C、D、E为短周期的主族元素,原子序数依次增大,其中有两种是金属元素,A、B两元素一起分别与C、D、E形成的三种最常见化合物两两之间均可发生反应,下列说法中正确的是( )
| A. | 原子半径:C>D>E>A>B | |
| B. | 常见氢化物的热稳定性:B<E | |
| C. | C可分别与A、B形成共价化合物、离子化合物 | |
| D. | 制备含D、E的二元化合物时,可能需要在无水条件下进行 |
13.化学与生产和生活密切相关.下列过程中没有发生化学变化的是( )
| A. | 氯气作自来水的杀菌消毒剂 | B. | 硅胶作袋装食品的干燥剂 | ||
| C. | 二氧化硫作纸浆的漂白剂 | D. | 大气中的NO2导致酸雨的形成 |
10.下列有关说法不正确的是( )
| A. | 苯与浓硝酸、浓硫酸共热并保持50~60℃反应生成硝基苯 | |
| B. | 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于苯环对侧链的影响,使侧链易被氧化 | |
| C. | 若甲苯苯环上的一个氢原子被一个含3个碳原子的烷基取代,所得产物有6种 | |
| D. | 菲的结构简式为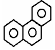 ,它与硝酸反应,可生成3种一硝基取代物 ,它与硝酸反应,可生成3种一硝基取代物 |
11.下列说法中正确的是( )
| A. | 金属单质在化学反应中只能做还原剂 | |
| B. | 非金属单质在化学反应中只能做氧化剂 | |
| C. | 金属原子在化学反应中失去的电子越多,其还原性就越强 | |
| D. | 置换反应不一定是氧化还原反应 |