题目内容
19.将下列粒子的序号填入相应空格内:①O2 ②CO2 ③H2O ④H2O2 ⑤(NH4)2SO4 ⑥SiCl4⑦C2H2 ⑧NH3 ⑨P4
只含有非极性键的非极性分子为①⑨;含极性键的非极性分子为②⑥⑦;
同时含有共价键、配位键、离子键的物质为⑤;正四面体分子为⑥⑨;
含极性键的极性分子为③④⑧;既含极性键,又含非极性键的极性分子为④.
分析 一般活泼金属元素与活泼非金属元素形成离子键;同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键;结构对称,正负电荷的中心重合,则为非极性分子;结构不对称,正负电荷的中心不重合,则为极性分子,据此分析.
解答 解:①O2 只含有非极性键,属于非极性分子;
②CO2 只含极性键,为直线形分子,结构对称为非极性分子;
③H2O 只含极性键,结构不对称,正负电荷的中心不重合,为极性分子;
④H2O2 含极性键和非极性键,结构不对称,正负电荷的中心不重合,为极性分子;
⑤(NH4)2SO4 含有共价键和离子键、配位键,属于离子化合物;
⑥SiCl4只含极性键,为正四面体结构,结构对称为非极性分子;
⑦C2H2含极性键和非极性键,为直线形分子,结构对称为非极性分子;
⑧NH3只含极性键,为三角锥形结构,结构不对称,正负电荷的中心不重合,为极性分子;
⑨P4只含非极性键,为正四面体结构,结构对称为非极性分子;
则只含有非极性键的非极性分子为①⑨;含极性键的非极性分子为②⑥⑦;
同时含有共价键、配位键、离子键的物质为⑤;正四面体分子为 ⑥⑨;
含极性键的极性分子为 ③④⑧;既含极性键,又含非极性键的极性分子为④;
故答案为:①⑨;②⑥⑦;⑤;⑥⑨;③④⑧;④.
点评 本题考查了键的极性和分子的极性,题目综合性较强,侧重于基础知识的考查,题目难度不大,注意掌握分子极性的判断方法.

练习册系列答案
相关题目
9.如表所示是元素周期表示意图的一部分,根据表中10种元素,用元素符号或化学式填空.
(1)①~⑩元素中,金属性最强的是K(填元素符号,下同);化学性质最不活泼是Ar.
(2)①~⑩元素中,最高价氧化物对应的水化物呈两性的元素是Al(填元素符号),该水化物与NaOH溶液反应的离子方程式为Al (OH)3+OH-=AlO2-+2H2O.
(3)①~⑩元素中,最高价氧化物对应的水化物的酸性最强的元素是Cl(填元素符号,下同),碱性最强的元素是K.
(4)⑤、⑥、⑧、⑨所形成的简单离子的半径由大到小的顺序是S2->Cl->K+>Ca2+.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅤⅠA | ⅤⅡA | O |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 四 | ⑧ | ⑨ | ⑩ |
(2)①~⑩元素中,最高价氧化物对应的水化物呈两性的元素是Al(填元素符号),该水化物与NaOH溶液反应的离子方程式为Al (OH)3+OH-=AlO2-+2H2O.
(3)①~⑩元素中,最高价氧化物对应的水化物的酸性最强的元素是Cl(填元素符号,下同),碱性最强的元素是K.
(4)⑤、⑥、⑧、⑨所形成的简单离子的半径由大到小的顺序是S2->Cl->K+>Ca2+.
10.胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得:101kPa时,H2的燃烧热为285.8kJ•mol-1,CH4的燃烧热为890.3kJ•mol-1.下列热化学方程式书写正确的是( )
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | $\frac{1}{2}$CH4(g)+O2(g)═$\frac{1}{2}$CO2(g)+H2O(l)△H=-445.15 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
7.设阿伏加德罗常数(NA)的数值为nA,下列说法不正确的是( )
| A. | 1mol Cl2与足量Fe反应,转移的电子数为2nA | |
| B. | 19.2g纯铜理论上可以制得纯净的硝酸铜的物质的量为0.3NA | |
| C. | 1.8 gAl与足量的盐酸反应放出的氢气为0.1NA | |
| D. | 0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10nA |
14.同周期的A、B、D三种元素,其最高价氧化物对应水化物的酸性强弱顺序是HAO4>H2BO4>H3DO4,则下列判断错误的是( )
| A. | 气态氢化物稳定性HA>H2B>DH3 | B. | 原子半径A>B>D | ||
| C. | 非金属性A>B>D | D. | 阴离子还原性B2->A- |
11.向盛有H2O2的试管中滴入一定量浓盐酸,有刺激性气味的气体生成.经实验证明该气体只含有O2、Cl2、HCl和水蒸气.将气体通入X溶液(如下图),依据观察到的现象,能判断气体中含有Cl2的是( )
| X溶液 | 现象 | 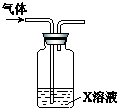 | |
| A | 紫色石蕊溶液 | 溶液先变红后褪色 | |
| B | 淀粉KI酸性溶液 | 溶液变为蓝色 | |
| C | 滴有KSCN的FeSO4溶液 | 溶液变为红色 | |
| D | 稀HNO3酸化的AgNO3溶液 | 有白色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
8.化学与人类的生活、生产息息相关,下列叙述正确的是( )
| A. | “春蚕到死丝方尽、蜡炬成灰泪始干”中的“丝”的主要成分是纤维素,属于天然高分子化合物 | |
| B. | “千锤万凿出深山,烈火焚烧若等闲”的过程中不但有物理变化,也有化学变化 | |
| C. | 日常生活中常用汽油去除衣物上的油污,用热的纯碱溶液洗涤炊具上的油污,两者的原理完全相同 | |
| D. | “84”消毒液的有效成分为NaClO,“洁厕灵”的有效成分为HCl,若将两者混合使用,其杀菌效果和去除厕所污渍的效果都将加强 |
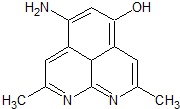 (1)第二周期元素中,第一电离能介于B和O之间的元素有Be、C.
(1)第二周期元素中,第一电离能介于B和O之间的元素有Be、C.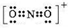 ,其等电子体有N2O、CO2(至少2种).
,其等电子体有N2O、CO2(至少2种).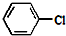 +2NaOH$\stackrel{加热加压}{→}$
+2NaOH$\stackrel{加热加压}{→}$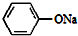 +NaCl+H2O
+NaCl+H2O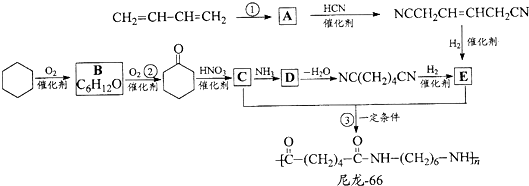
 .
. 、
、 ;
; .
.