题目内容
1.下列选项中的各操作,能使原溶液导电性明显变强的是( )| A. | 向0.1mol/L的NaOH溶液中加入等体积的0.1mol/L的HCl溶液 | |
| B. | 向0.1mol/L的NaOH溶液中加入等体积的0.1mol/L的CH3COOH溶液 | |
| C. | 向0.1mol/L的Ba(OH)2溶液中加入等体积的0.1mol/L的H2SO4溶液 | |
| D. | 向0.1mol/L的NH3•H2O溶液中加入等体积的0.1mol/L的CH3COOH溶液 |
分析 电解质溶液导电性与离子浓度成正比,电解质溶液中离子浓度明显增大,则溶液导电性就明显增强,据此分析解答.
解答 A.NaOH、HCl、NaCl都是强电解质,在水溶液中完全电离,向0.1mol/L的NaOH溶液中加入等体积的0.1mol/L的HCl溶液,离子浓度减小,溶液导电性减弱,故A错误;
B.NaOH是强电解质、醋酸钠是强电解质,向0.1mol/L的NaOH溶液中加入等体积的0.1mol/L的CH3COOH溶液,混合溶液中离子浓度减小,溶液导电性减弱,故B错误;
C.氢氧化钡、硫酸、硫酸钡都是强电解质,但硫酸钡溶解性较小,向0.1mol/L的Ba(OH)2溶液中加入等体积的0.1mol/L的H2SO4溶液,二者恰好反应生成硫酸钡和水,混合溶液中离子浓度很小,导电性很弱,故C错误;
D.一水合氨、醋酸是弱电解质,醋酸铵是强电解质,向0.1mol/L的NH3•H2O溶液中加入等体积的0.1mol/L的CH3COOH溶液,混合溶液中离子浓度明显增大,溶液导电性明显增强,故D正确;
故选D.
点评 本题考查电解质溶液导电性强弱判断,为高频考点,明确电解质溶液导电性与离子浓度关系是解本题关键,易错选项是C,虽然硫酸钡是强电解质,但其溶解度很小,导致硫酸钡溶液导电性很弱,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列关于安全方面叙述不正确的是( )
| A. | Na2O2属于危险化学品,其标识应为: | |
| B. | 当你走进化学实验室之前,应认真阅读实验室的安全守则 | |
| C. | 中国大陆的火警报警电话为“119”,香港、澳门为“999” | |
| D. | 一般情况下,金属类物质着火时不宜使用二氧化碳类灭火器 |
6.工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如图:
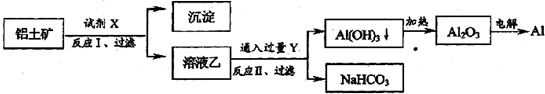
对上述流程中的判断正确的是( )

对上述流程中的判断正确的是( )
| A. | 试剂X为稀硫酸 | |
| B. | 反应II中生成Al(OH)3的反应为:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| C. | 结合质子( H+)的能力由强到弱的顺序是:OH->HCO3->AlO2- | |
| D. | Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al |
11.酸雨、臭氧层被破坏、温室效应和土地荒漠化是当今人类面临的严重环境问题.下列说法中错误的是( )
| A. | 在冰箱中使用含氟致冷剂,会破坏臭氧层 | |
| B. | 大量使用矿物燃料会导致温室效应 | |
| C. | 大量含硫燃料的燃烧会导致酸雨的增多 | |
| D. | 气侯变暖是导致土地荒漠化的主要原因 |