题目内容
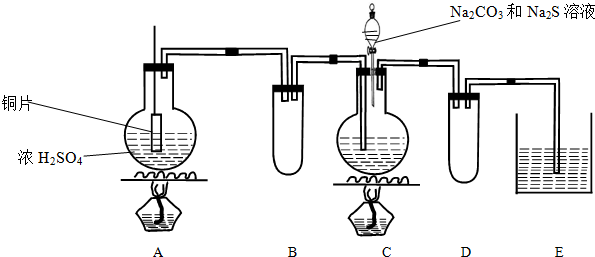
5.钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁(FeTiO)3,还含有少量Fe2O3]为原料制备钛的工艺流程如图所示: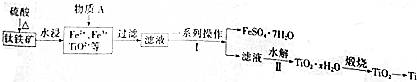
(1)钛铁矿与硫酸反应的主要反应的化学方程式为FeTiO3+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$TiOSO4+FeSO4+2H2O.
(2)物质A为Fe(填化学式),步骤Ⅰ中的“一系列操作”为蒸发浓缩、冷却结晶、过滤.
(3)步骤Ⅱ中发生反应的离子方程式为TiO2++(x+1)H2O═TiO2•xH2O↓+2H+;为提高TiO2•xH2O的产率,可采取的措施有加水稀释反应物、加碱中和生成的酸、加热等(写出两条)
(4)由TiO2获得Ti可用以下两种方法.
①电解法:以石墨为阳极,TiO2为阴极,熔融CaO为电解质,其阴极的电极反应式为TiO2+4e-═Ti+2O2-.
②热还原法:首先将TiO2、氯气和过量焦炭混合,高温反应生成TiCl4;然后用Mg还原TiCl4即可制取Ti.生成TiCl4的反应中,氧化剂与还原剂的物质的量之比为1:1;生成Ti的反应需在Ar气氛中,其原因为防止高温下Mg(或Ti)与空气中的O2(或CO2、N2)反应.
分析 根据题中流程可知,钛铁矿[主要成分为钛酸亚铁(FeTiO)3,加硫酸溶解生成TiO2+和Fe3+、Fe2+等,再加铁粉还原Fe3+,过滤除去滤渣,将滤液蒸发浓缩、冷却结晶、过滤得到FeSO4•7H2O晶体和含有TiO2+的溶液,TiO2+经过水解得TiO2•xH2O,TiO2•xH2O再煅烧得TiO2,将TiO2还原可得Ti,据此答题.
解答 解:根据题中流程可知,钛铁矿[主要成分为钛酸亚铁(FeTiO)3,加硫酸溶解生成TiO2+和Fe3+、Fe2+等,再加铁粉还原Fe3+,过滤除去滤渣,将滤液蒸发浓缩、冷却结晶、过滤得到FeSO4•7H2O晶体和含有TiO2+的溶液,TiO2+经过水解得TiO2•xH2O,TiO2•xH2O再煅烧得TiO2,将TiO2还原可得Ti,
(1)钛铁矿与硫酸反应的主要反应的化学方程式为FeTiO3+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$TiOSO4+FeSO4+2H2O,
故答案为:FeTiO3+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$TiOSO4+FeSO4+2H2O;
(2)根据上面的分析可知,物质A为 Fe,步骤Ⅰ是从含有硫酸亚铁的溶液中获得硫酸亚铁晶体,所以步骤Ⅰ中的“一系列操作”为蒸发浓缩、冷却结晶、过滤,
故答案为:Fe;蒸发浓缩、冷却结晶、过滤;
(3)步骤Ⅱ中TiO2+经过水解得TiO2•xH2O,发生反应的离子方程式为TiO2++(x+1)H2O═TiO2•xH2O↓+2H+,为提高TiO2•xH2O的产率,可采取的措施有加水稀释反应物、加碱中和生成的酸、加热等,
故答案为:TiO2++(x+1)H2O═TiO2•xH2O↓+2H+;加水稀释反应物、加碱中和生成的酸、加热等;
(4)①电解TiO2获得Ti,用TiO2为阴极,其阴极的电极反应式为TiO2+4e-═Ti+2O2-,
故答案为:TiO2+4e-═Ti+2O2-;
②将TiO2、氯气和过量焦炭混合,高温反应生成TiCl4,反应的方程式为TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO,根据方程式可知,反应中氯气为氧化剂,碳为还原剂,氧化剂与还原剂的物质的量之比为1:1,由于钛和镁在与空气在高温反应所以反应需在Ar气氛中,
故答案为:1:1;防止高温下Mg(或Ti)与空气中的O2(或CO2、N2)反应.
点评 本题考查了物质制备流程分析判断,实验基本操作,离子方程式的书写,数据计算等,题目涉及的知识点较多,综合性强,考查学生对所学知识的综合应用能力,题目难度中等.

| A. | 给试管里的液体加热,液体的体积一般不超过试管容积的$\frac{1}{2}$ | |
| B. | 向酒精灯里添加酒精,不可超过酒精灯容积的$\frac{2}{3}$ | |
| C. | 酒精灯使用完毕,应立即用嘴吹灭火焰 | |
| D. | 用燃着的酒精灯去点燃另一盏酒精灯 |
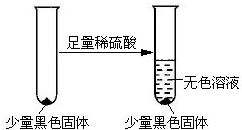
Ⅰ、向一定量样品中加入过量盐酸,产生气体A.
Ⅱ、向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤.
Ⅲ、向沉淀B中加过量NaOH溶液,沉淀全部溶解.
Ⅳ、向Ⅱ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C.
已知:Al3+在pH=5.0时沉淀完全:Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全.且有n(A):n(B):n(C)=2:2:3,则该碱式碳酸铝镁的化学式为( )
| A. | Mg2Al2(OH)4(CO3)3 | B. | Mg3Al2(OH)6(CO3)2 | C. | Mg3Al(OH)3(CO3)3 | D. | Mg3Al2(OH)8(CO3)2 |
| A. | 金属铁与过量的稀盐酸反应:2Fe+6H+→2Fe3++3H2↑ | |
| B. | 氯化亚铁溶液中通入少量氯气:Fe2++Cl2→Fe3++2Cl- | |
| C. | 氧化铝与氢氧化钠溶液反应:Al2O3+2OH-=2AlO2-+H2O | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++3OH-→Al(OH)3↓ |
| A. | 将“地沟油”反应改性制成“生物柴油”,代替柴油作为内燃机燃料的做法符合“绿色化学”的理念 | |
| B. | 红宝石、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 | |
| C. | 科学家推测月尘[即月球上直径小于10微米(1μm=1×10-6m)的浮尘]是“玉兔号”出现控制异常情况的主要原因,月尘在空气中形成的分散系不属于胶体 | |
| D. | “煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 |
| A. | 碘化钾 | B. | 碘化银 | C. | 溴化银 | D. | 氯水 |
| A. | 1mol氯气参加氧化还原反应时电子转移数一定是2NA | |
| B. | 常温常压下,56 g Fe与足量的盐酸完全反应转移的电子数为3NA | |
| C. | 同温同压下,等质量的H2和O2的体积之比是16:1 | |
| D. | 0.1mol/L的MgCl2溶液中Cl-离子数为2NA |