题目内容
下列溶液中,c(Cl-)最小的是( )
| A、20mL 0.5mol/L AlCl3溶液 |
| B、30mL 1mol/L KCl溶液 |
| C、7.5mL 2mol/L MgCl2溶液 |
| D、10mL 3mol/L NaCl溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:电解质离子浓度=电解质浓度×电解质电离出的该离子数目,注意离子的物质的量浓度与溶液的体积无关,据此结合选项计算判断.
解答:
解:A、20mL 0.5mol/L AlCl3溶液中,c(Cl-)=0.5mol/L×3=1.5mol/L;
B、30mL1mol/L KCl 溶液中,c(Cl-)=1mol/L×1=1mol/L;
C、7.5mL 2mol/L MgCl2溶液中,c(Cl-)=2mol/L×2=4mol/L;
D、10mL 3mol/L NaCl溶液中,c(Cl-)=3mol/L×1=3mol/L;
所以Cl-浓度最小的是B,
故选B.
B、30mL1mol/L KCl 溶液中,c(Cl-)=1mol/L×1=1mol/L;
C、7.5mL 2mol/L MgCl2溶液中,c(Cl-)=2mol/L×2=4mol/L;
D、10mL 3mol/L NaCl溶液中,c(Cl-)=3mol/L×1=3mol/L;
所以Cl-浓度最小的是B,
故选B.
点评:本题考查了物质的量浓度概念的分析判断,注意物质浓度和离子浓度的分析应用,关键是溶液中是否存在氯离子,题目较简单

练习册系列答案
相关题目
在相同温度和压强下,1mol Ar和1mol NH3具有相同的( )
| A、分子数 | B、质量 |
| C、原子数 | D、体积 |
 下列关于如图所示的原电池的有关说法中,正确的是( )
下列关于如图所示的原电池的有关说法中,正确的是( )| A、铜棒发生氧化反应 |
| B、锌棒上有气泡产生 |
| C、锌棒质量减轻 |
| D、电子从铜棒经外电路流向锌棒 |
下列化学用语错误的是( )
A、氯化氢分子的电子式: | ||
B、硫离子的结构示意图: | ||
C、中子数为8的碳原子:
| ||
| D、二氧化碳的结构式:O=C=O |
 化学是以实验为基础的学科,下列有关实验的描述正确的是( )
化学是以实验为基础的学科,下列有关实验的描述正确的是( )| A、向两支分别装有碳酸钠和碳酸氢钠固体的试管中各加几滴水,前者温度降低,后者温度升高 |
| B、向100mL容量瓶中加入4.0gNaOH固体,然后加水到刻度线,配制1.0mol/L的NaOH溶液 |
| C、向酸性重铬酸钾溶液中加NaOH,溶液颜色由橙色慢慢变为黄色 |
| D、如图所示,随着空气的通入,试管内液面会慢慢上升至充满整支试管,而后液面又下降. |
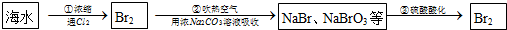
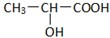 .试回答:
.试回答: