题目内容
13.前4周期元素A、B、C、D、E、F,原子序数依次增大,其中A和B同周期,固态的AB2能升华,常用作致冷剂;C和E原子都有一个未成对电子,C+比E-少一个电子层,E原子得一个电子后3p轨道全充满;D的最高化合价和最低化合价代数和为4,F为红色单质,日常生活中常见的金属元素.回答下列问题:
(1)元素电负性:D<E;A、C单质熔点:A>C(填“>”、“<”或“=”).
(2)AE4常用作有机溶剂,其固态晶体类型为分子晶体.
(3)B的氢化物的沸点高于D的氢化物,其原因是H2O形成分子间氢键,而H2S分子间只有范德华力
(4)有关资料报道:在40GPa高压下,将AB2用激光器加热到1800K,制得了一种与二氧化硅晶体类似的高熔点、高硬度的晶体,下列关于该晶体的说法不正确的是D
A、该晶体属于原子晶体
B、该晶体中碳氧键的键角可为109°28’
C、该晶体中碳、氧原子的最外层都是8个电子
D、每摩该晶体中含2mol σ键
(5)F的核外电子排布式为1s22s22p63s23p63d104s1;向F的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,请根据实验现象写出有关反应的离子方程式
(1)Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+
(2)Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
分析 前四周期元素A、B、C、D、E、F,原子序数依次增大,A和B同周期,固态的AB2能升华,AB2为CO2,则A为碳元素,B为氧元素;E原子的一个电子后3p轨道全充满,则E最外层电子数为7,故E为氯元素;C和E原子都有一个未成对电子,C+比E-少一个电子层,则C为钠元素;D的最高化合价和最低化合价代数和为4,D最外层电子数为6,D原子序数大于钠元素小于氯元素,故D为硫元素;F为红色单质,广泛用于电气工业,F为铜元素.
(1)同周期自左而右,元素电负性增强;碳单质金刚石为原子晶体,熔点很高,钠为金属晶体且熔点较低;
(2)CCl4常用作有机溶剂,其固态晶体类型为分子晶体;
(3)H2O形成分子间氢键,而H2S分子间只有范德华力;
(4)在40GPa高压下,将CO2用激光器加热到1800K,制得了一种与二氧化硅晶体类似的高熔点、高硬度的晶体,该CO2晶体属于原子晶体,碳原子与周围的4个O原子形成正四面体结构,每个O原子与2个C原子形成共价键;
(5)Cu原子核外电子数为29,根据核外电子排布规律书写电子排布式;向硫酸铜中逐滴加入氨水先产生氢氧化铜沉淀,后沉淀溶解生成[Cu(NH3)4]2+,溶液呈深蓝色溶液.
解答 解:前四周期元素A、B、C、D、E、F,原子序数依次增大,A和B同周期,固态的AB2能升华,AB2为CO2,则A为碳元素,B为氧元素;E原子的一个电子后3p轨道全充满,则E最外层电子数为7,故E为氯元素;C和E原子都有一个未成对电子,C+比E-少一个电子层,则C为钠元素;D的最高化合价和最低化合价代数和为4,D最外层电子数为6,D原子序数大于钠元素小于氯元素,故D为硫元素;F为红色单质,广泛用于电气工业,F为铜元素.
(1)D为硫元素,E为氯元素,同周期自左而右,元素电负性增强,所以电负性D<E;
A为碳元素,C为Na,碳单质金刚石为原子晶体,熔点很高,钠为金属晶体且熔点较低,所以熔点A>C.
故答案为:>;<;
(2)CCl4常用作有机溶剂,其固态晶体类型为分子晶体,
故答案为:分子晶体;
(3)H2O形成分子间氢键,而H2S分子间只有范德华力,则水的沸点高于硫化氢的,
故答案为:H2O形成分子间氢键,而H2S分子间只有范德华力;
(4)A.40GPa高压下,将CO2用激光器加热到1800K,制得了一种与二氧化硅晶体类似的高熔点、高硬度的晶体,该CO2晶体属于原子晶体,故A正确;
B.碳原子与周围的4个O原子形成正四面体结构,晶体中碳氧键的键角可为109°28’,故B正确;
C.碳原子与周围的4个O原子形成共价键,每个O原子与2个C原子形成共价键,该晶体中碳、氧原子的最外层都是8个电子,故C正确;
D.每个碳原子形成4个σ键,每摩该晶体中含4mol σ键,故D错误,
故选:D;
(5)Cu原子核外电子数为29,核外电子排布式为1s22s22p63s23p63d104s1,向硫酸铜中逐滴加入氨水先产生氢氧化铜沉淀,后沉淀溶解生成[Cu(NH3)4]2+,溶液呈深蓝色溶液,反应离子方程式为:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-,
故答案为:1s22s22p63s23p63d104s1;Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+;Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
点评 本题是对物质结构与性质的考查,涉及电子排布式、电负性、晶体类型与性质、氢键、晶体结构、配合物等,注意氢键对物质性质的影响,难度中等.

 习题精选系列答案
习题精选系列答案
实验(一):乳酸的制取
步骤1:取14.40g葡萄糖(相对分子质量为180于烧杯中,加入乳酸菌(厌氧)发酵,72小时后,过滤,将滤液转移到仪器A中,定容,得到500mL原液;
步骤2:取20.00mL原液于锥形瓶中,加入酚酞作指示剂,用浓为0.1000mol/L的NaOH溶液滴定至终点,重复4次,数据记录如下表.(假定原液中其他物质不与NaOH反应)
| 次数 | 1 | 2 | 3 | 4 |
| 滴定体积(mL) | 19.22 | 19.18 | 19.80 | 19.20 |
(2)如何判断已到达滴定终点当滴入最后一滴标准液时,锥形瓶中无色溶液变红色,且半分钟内不褪色;
(3)乳酸的产率为30%.
实验(二):乳酸的性质
已知乳酸的Ka=1.4×10-4,碳酸的Ka1=4.47×10-3
(4)设计实验证明乳酸是弱酸:取0.1mol/L乳酸溶液于烧杯中,用PH计测定其PH值,若PH大于1,说明乳酸是弱酸或(常温下取0.1mol/L乳酸钠溶液于烧杯中,用pH计测定其PH值,若PH大于7,说明乳酸是弱酸)或(取PH=a乳酸溶液于烧杯中,加水稀释10n倍,用PH计测定其PH值,若PH小于a+n说明乳酸是弱酸).
(5)小组利用如图所示的仪器和药品,通过实验来比较乳酸与碳酸的酸性强弱.

①可观察到烧杯中的现象是溶液出现白色浑浊;写出烧杯中发生的化学反应方程式2NaAlO2+3H2O+CO2═2Al(OH)3↓+Na2CO3或NaAlO2+2H2O+CO2═Al(OH)3↓+NaHCO3;
②学习小组中有成员提出上述实验设计不够严谨,请你提出改进的措施在A与B之间增加一个装有碳酸氢钠溶液的洗气瓶.
| A. | 氯气与氢气化合比溴与氢气化合容易 | |
| B. | 硒化氢比硫化氢稳定 | |
| C. | 氢氧化锶比氢氧化钙的碱性强 | |
| D. | 铍的原子失电子能力比镁弱 |
| A. | 被氧化的砒霜为1.98mg | B. | 分解产生的氢气为0.672ml | ||
| C. | 转移的电子总数为0.18NA | D. | 和砒霜反应的锌为3.90mg |
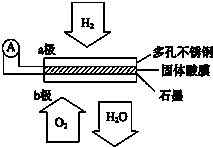 某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是( )
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是( )| A. | 电子通过外电路从b极流向a极 | |
| B. | b极上的电极反应式为:O2+2H2O+4e-=4OH- | |
| C. | 每转移0.1 mol电子,消耗标准状况下1.12 L的H2 | |
| D. | OH-由a极通过固体酸电解质传递到b极 |
| A. | 70 | B. | 114 | C. | 184 | D. | 289 |
 ,氢元素含量最高的烃的分子式CH4.
,氢元素含量最高的烃的分子式CH4.
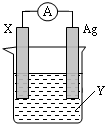 依据氧化还原反应:2Ag+(aq)+Zn(s)=Zn2+(aq)+2Ag(s) 设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Zn(s)=Zn2+(aq)+2Ag(s) 设计的原电池如图所示.请回答下列问题: