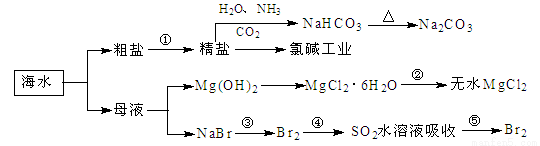
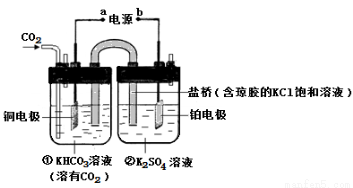
题目内容
①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,不正确的是( )
A.水电离的c(H+):①=②=③=④
B.若将②、③溶液混合后,pH=7,则消耗溶液的体积:②>③
C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大
D.向溶液中加入100mL水后,溶液的pH:③>④>②>①
C
【解析】
试题分析:A、四种溶液中,①、②的氢离子浓度相等,③、④的氢氧根离子浓度相等,所以对水的电离的抑制作用相同,则水电离的c(H+):①=②=③=④,正确;B、②、③溶液中的氢离子浓度癒氢氧根离子浓度相等,但氨水是弱碱溶液,所以溶液的浓度大于HCl溶液的浓度,等体积混合,氨水过量,这溶液呈碱性,现在溶液呈中性,则盐酸的体积大,②>③,正确;C、①、②、④相比溶液中的氢离子与氢氧根离子的浓度相等,但醋酸是弱酸,溶液的浓度远大于盐酸的浓度,而Al与氢氧化钠溶液反应时2OH-~3H2,2H+~H2,所以②生成的氢气的量最少,错误;D、氨水是弱碱溶液,加水稀释后溶液的pH减小的少,所以pH:③>④,同理醋酸加水稀释后溶液的pH的增大比盐酸增大的少,酸性最强,所以溶液的pH:③>④>②>①,正确,答案选C。
考点:考查溶液的pH与溶液浓度的关系的判断

下列实验方案中,不能达到实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |

 2NH3
2NH3 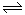 4NH3(g)+3O2(g) △H=Q ①
4NH3(g)+3O2(g) △H=Q ①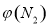 与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。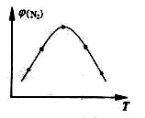
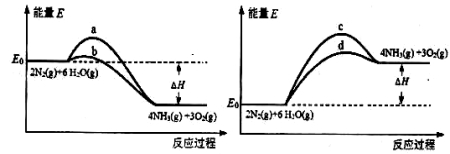
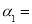 ______________。
______________。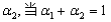 时,则起始时NH3的物质的量
时,则起始时NH3的物质的量 _________mol。
_________mol。