题目内容
在常温下,下列五种溶液:
①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4 ③0.1mol/L NH4HSO4
④0.1mol/L NH3?H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3?H2O
请根据要求填写下列空白:
(1)溶液①呈 性(填“酸”、“碱”或“中”),其原因是 (用离子方程式表示)
(2)上述五种溶液中,pH最小的是 ;由水电离出c(H+)最小的是 (填序号)
(3)比较溶液②、③中c(NH4+)的大小关系是② ③(填“>”、“<”或“=”)
(4)在溶液④中, 离子的浓度为0.1mol/L;NH3?H2O和 离子的物质的量浓度之和为0.2mol/L
(5)常温下,测得溶液②的pH=7,则 CH3COO-与NH4+浓度的大小关系是:c(CH3COO-) c(NH4+)(填“>”、“<”或“=”)
(6)⑤溶液呈碱性的原因是 (用离子方程式表示)
①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4 ③0.1mol/L NH4HSO4
④0.1mol/L NH3?H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3?H2O
请根据要求填写下列空白:
(1)溶液①呈
(2)上述五种溶液中,pH最小的是
(3)比较溶液②、③中c(NH4+)的大小关系是②
(4)在溶液④中,
(5)常温下,测得溶液②的pH=7,则 CH3COO-与NH4+浓度的大小关系是:c(CH3COO-)
(6)⑤溶液呈碱性的原因是
考点:盐类水解的应用
专题:盐类的水解专题
分析:(1)氯化铵是强酸弱碱盐,铵根离子水解导致溶液呈酸性;
(2)硫酸氢铵溶液呈强酸性,pH最小,酸或碱抑制水电离,含有弱离子的盐促进水电离;
(3)氢离子抑制铵根离子水解、弱酸根离子促进铵根离子水解;
(4)任何电解质溶液中都存在物料守恒,根据物料守恒判断;
(5)常温下,测得溶液②的pH=7,根据电荷守恒判断CH3COO-与NH4+浓度的大小关系;
(6)一水合氨电离生成氢氧根离子而使溶液呈碱性.
(2)硫酸氢铵溶液呈强酸性,pH最小,酸或碱抑制水电离,含有弱离子的盐促进水电离;
(3)氢离子抑制铵根离子水解、弱酸根离子促进铵根离子水解;
(4)任何电解质溶液中都存在物料守恒,根据物料守恒判断;
(5)常温下,测得溶液②的pH=7,根据电荷守恒判断CH3COO-与NH4+浓度的大小关系;
(6)一水合氨电离生成氢氧根离子而使溶液呈碱性.
解答:
解:(1)氯化铵是强酸弱碱盐,铵根离子水解导致溶液呈酸性,水解方程式为NH4++H2O?NH3.H2O+OH-,故答案为:酸;NH4++H2O?NH3.H2O+OH-;
(2)硫酸氢铵完全电离生成氢离子、铵根离子和硫酸根离子,导致溶液呈强酸性,pH最小,酸或碱抑制水电离,含有弱离子的盐促进水电离,所以由水电离出c(H+)最小的是一水合氨溶液,故答案为:③;⑤;
(3)氢离子抑制铵根离子水解、弱酸根离子促进铵根离子水解,所以溶液②、③中c(NH4+)的大小关系是②<③,故答案为:<;
(4)任何电解质溶液中都存在物料守恒,根据物料守恒得c(Cl-)=0.1mol/L,c(NH3)+c(NH4+)=0.2mol/L,故答案为:Cl-;NH4+;
(5)常温下,测得溶液②的pH=7,则c(OH-)=c(H+),根据电荷守恒得c(CH3COO-)=c(NH4+),故答案为:=;
(6)一水合氨电离生成氢氧根离子而使溶液呈碱性,电离方程式为NH3.H2O?NH4++OH-,故答案为:NH3.H2O?NH4++OH-.
(2)硫酸氢铵完全电离生成氢离子、铵根离子和硫酸根离子,导致溶液呈强酸性,pH最小,酸或碱抑制水电离,含有弱离子的盐促进水电离,所以由水电离出c(H+)最小的是一水合氨溶液,故答案为:③;⑤;
(3)氢离子抑制铵根离子水解、弱酸根离子促进铵根离子水解,所以溶液②、③中c(NH4+)的大小关系是②<③,故答案为:<;
(4)任何电解质溶液中都存在物料守恒,根据物料守恒得c(Cl-)=0.1mol/L,c(NH3)+c(NH4+)=0.2mol/L,故答案为:Cl-;NH4+;
(5)常温下,测得溶液②的pH=7,则c(OH-)=c(H+),根据电荷守恒得c(CH3COO-)=c(NH4+),故答案为:=;
(6)一水合氨电离生成氢氧根离子而使溶液呈碱性,电离方程式为NH3.H2O?NH4++OH-,故答案为:NH3.H2O?NH4++OH-.
点评:本题考查了盐类水解和弱电解质的电离,知道常见弱电解质、盐的性质是解本题关键,知道弱酸酸性强弱与酸根离子水解程度关系,注意硫酸氢铵电离方式,题目难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
下列有关说法正确的是( )
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | ||
| B、电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | ||
C、CH3COOH 溶液加水稀释后,溶液中
| ||
| D、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |

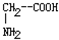 和丙氨酸
和丙氨酸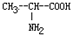 混合反应,生成的“二肽”最多为
混合反应,生成的“二肽”最多为