题目内容
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | 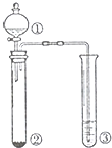 |
| A | 浓硫酸 | Cu | 品红溶液 | SO2具有漂白性 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、 氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3 溶液 | 酸性:硝酸>碳酸 >硅酸 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,硝酸的化学性质,二氧化硫的化学性质,浓硫酸的性质,实验装置综合
专题:实验设计题,实验评价题
分析:A.浓硫酸与铜的反应应在加热条件下进行;
B.浓硫酸使蔗糖变黑,然后C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应使其褪色;
C.盐酸与亚硫酸钠生成二氧化硫,与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡沉淀;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与硅酸钠溶液反应生成硅酸沉淀.
B.浓硫酸使蔗糖变黑,然后C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应使其褪色;
C.盐酸与亚硫酸钠生成二氧化硫,与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡沉淀;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与硅酸钠溶液反应生成硅酸沉淀.
解答:
解:A.浓硫酸与铜的反应应在加热条件下进行,图中没有加热,不能生成二氧化硫,故A错误;
B.浓硫酸具有脱水性使蔗糖变黑,然后C与浓硫酸发生氧化还原反应生成二氧化硫,体现其强氧化性,最后二氧化硫与溴水发生氧化还原反应使其褪色,故B正确;
C.盐酸与亚硫酸钠生成二氧化硫,与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡沉淀,但SO2与可溶性钡盐不一定生成白色沉淀,如与氯化钡不反应,故C错误;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与硅酸钠溶液反应生成硅酸沉淀,则不能比较碳酸与硅酸的酸性,应排除硝酸的干扰,故D错误;
故选B.
B.浓硫酸具有脱水性使蔗糖变黑,然后C与浓硫酸发生氧化还原反应生成二氧化硫,体现其强氧化性,最后二氧化硫与溴水发生氧化还原反应使其褪色,故B正确;
C.盐酸与亚硫酸钠生成二氧化硫,与Ba(NO3)2溶液发生氧化还原反应生成硫酸钡沉淀,但SO2与可溶性钡盐不一定生成白色沉淀,如与氯化钡不反应,故C错误;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与硅酸钠溶液反应生成硅酸沉淀,则不能比较碳酸与硅酸的酸性,应排除硝酸的干扰,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及浓硫酸的性质、酸性比较、氧化还原反应等,把握化学反应原理及实验装置中的反应为解答的关键,注意实验操作的可行性、评价性分析,题目难度不大.

练习册系列答案
相关题目
已知HCN的电离常数Ka=5×10-10,H2CO3离常数Ka1=4.3×10-7、Ka2=5.6×10-11,判断在等浓度的NaCN、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A、c(HCO3-)>c(CN- )>c(OH- ) |
| B、c(CN- )>c(HCO3-)>c(H+ ) |
| C、c(HCN)+c(CN- )=c(HCO3-)+c(H2CO3) |
| D、c(Na+ )+c(H+ )=c(HCO3- )+c(CN- )+C(OH- ) |
已知氧化性Br2>Fe3+.FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:aFe2++bBr-+cCl2═dFe3++eBr2+fCl-下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A、2 6 4 2 3 8 |
| B、2 4 3 2 2 6 |
| C、2 0 1 2 0 2 |
| D、2 2 2 2 1 4 |
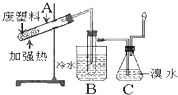 加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,用图所示装置探究废旧塑料的再利用.下列叙述不正确的是( )
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,用图所示装置探究废旧塑料的再利用.下列叙述不正确的是( )| A、丙烯分子中共用电子对数为10 |
| B、装置B的试管中可收集到芳香烃 |
| C、装置C中的试剂可吸收烯烃以制取卤代烃 |
| D、最后收集的气体可做燃料 |
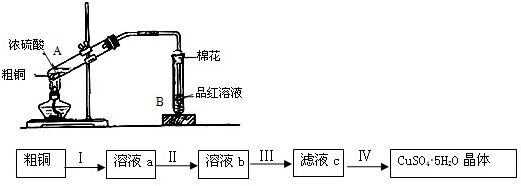
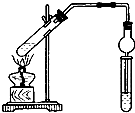 用如图所示实验装置制取乙酸乙酯.回答以下问题:
用如图所示实验装置制取乙酸乙酯.回答以下问题: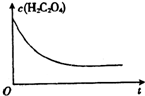 某合作小组同学在进行酸性高锰酸钾溶液与草酸(化学式为H2C2O4,被氧化为CO2)溶液的反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快.该小组通过实验探究其原因.
某合作小组同学在进行酸性高锰酸钾溶液与草酸(化学式为H2C2O4,被氧化为CO2)溶液的反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快.该小组通过实验探究其原因.