题目内容
(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式 .
(2)用如图所示装置可检验木炭和浓硫酸反应产生的混合气体中含有SO2和CO2.
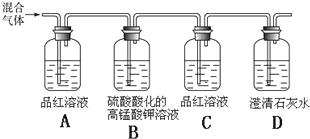
①能够证明混合气体中含有SO2的实验现象是: ;
②设计B、C的实验目的是: ;
③写出B中发生反应的离子方程式: ;
④能够证明混合气体中含有CO2的实验现象是: .
(2)用如图所示装置可检验木炭和浓硫酸反应产生的混合气体中含有SO2和CO2.

①能够证明混合气体中含有SO2的实验现象是:
②设计B、C的实验目的是:
③写出B中发生反应的离子方程式:
④能够证明混合气体中含有CO2的实验现象是:
考点:浓硫酸的性质实验
专题:氧族元素
分析:(1)碳与浓硫酸在加热条件下反应生成二氧化碳、二氧化硫气体和水;
(2)①二氧化硫具有漂白性,如果A中品红溶液褪色,证明混合气体中含有二氧化硫气体;
②二氧化硫也能够使澄清石灰水变浑浊,若要检验二氧化碳,应该先用酸性高锰酸钾除去二氧化硫,再用品红溶液检验二氧化硫是否除尽;
③B中二氧化硫被酸性高锰酸钾溶液氧化成硫酸根离子;
④若C中品红溶液不褪色而D中澄清石灰水变浑浊则证明混合气体中含有二氧化碳.
(2)①二氧化硫具有漂白性,如果A中品红溶液褪色,证明混合气体中含有二氧化硫气体;
②二氧化硫也能够使澄清石灰水变浑浊,若要检验二氧化碳,应该先用酸性高锰酸钾除去二氧化硫,再用品红溶液检验二氧化硫是否除尽;
③B中二氧化硫被酸性高锰酸钾溶液氧化成硫酸根离子;
④若C中品红溶液不褪色而D中澄清石灰水变浑浊则证明混合气体中含有二氧化碳.
解答:
解:(1)碳与浓硫酸反应生成生成二氧化硫、二氧化碳和水,反应的化学方程式为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,
故答案为:2H2SO4(浓)+C
CO2↑+SO2↑+2H2O;
(2)①二氧化硫具有漂白性,若装置A中品红溶液褪色,则证明混合气体中存在二氧化硫,
故答案为:A中品红溶液褪色;
②由于二氧化硫能够使澄清石灰水变浑浊,为了排除检验二氧化碳时二氧化硫的干扰,用酸性高锰酸钾溶液除去二氧化硫,然后用品红溶液检验二氧化硫已经除尽,
故答案为:除去SO2并检验SO2,气体是否除尽,排除SO2对CO2气体检验的干扰;
③B中酸性高锰酸钾溶液具有强氧化性,能够将二氧化硫氧化成硫酸根离子,反应的离子方程式为:5SO2+2MnO4-+2H2O=5 SO42-+2Mn2++4H+,
故答案为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
④C中品红溶液不褪色,证明混合气体中的二氧化硫已经完全除去,若D中澄清石灰水变浑浊,则证明混合气体中含有二氧化碳气体,
故答案为:C中品红溶液不褪色D中溶液变浑浊.
| ||
故答案为:2H2SO4(浓)+C
| ||
(2)①二氧化硫具有漂白性,若装置A中品红溶液褪色,则证明混合气体中存在二氧化硫,
故答案为:A中品红溶液褪色;
②由于二氧化硫能够使澄清石灰水变浑浊,为了排除检验二氧化碳时二氧化硫的干扰,用酸性高锰酸钾溶液除去二氧化硫,然后用品红溶液检验二氧化硫已经除尽,
故答案为:除去SO2并检验SO2,气体是否除尽,排除SO2对CO2气体检验的干扰;
③B中酸性高锰酸钾溶液具有强氧化性,能够将二氧化硫氧化成硫酸根离子,反应的离子方程式为:5SO2+2MnO4-+2H2O=5 SO42-+2Mn2++4H+,
故答案为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
④C中品红溶液不褪色,证明混合气体中的二氧化硫已经完全除去,若D中澄清石灰水变浑浊,则证明混合气体中含有二氧化碳气体,
故答案为:C中品红溶液不褪色D中溶液变浑浊.
点评:本题考查了浓硫酸的化学性质,题目难度中等,侧重考查浓硫酸与铜的反应及二氧化硫的性质,注意明确检验二氧化碳的存在时,需要排除二氧化硫的干扰,试题培养了学生的分析、理解能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在某容积一定的决斗容器中,有下列可逆反应2A(g)+B(g)?xC(g),反应曲线(T表示温度,P表示压强,C% 表示C的体积分数)如图所示,试判断对图的说法中正确的是( )
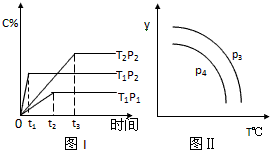

| A、x=2 |
| B、该反应是吸热反应 |
| C、P3>P4,y轴表示B的转化率 |
| D、P3<P4,y轴表示混合气体的密度 |
NA为阿伏伽德罗常数,下列叙述正确的是( )
| A、18gH2O中含有的质子数为NA |
| B、常温常压下,Na2O2与足量H2O反应,每生成1 molO2,转移电子的数目为4NA |
| C、46gNO2和N2O4混合气体中含有原子总数为3NA |
| D、物质的量浓度为0.5 mol?L-1的MgCl2的溶液中,含有Cl-个数为NA |
下列化学用语的表示正确的是( )
A、CS2的比例模型: |
| B、乙醇的结构简式:C2H6O |
| C、核内有8个中子的碳原子:86C |
| D、HClO的结构简式:H-Cl-O |
下列离子方程式错误的是( )
| A、灭火器中盛装的是Al2(SO4)3溶液和NaHCO3溶液,使用时把两者混合即可生成CO2:Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
| B、Al(OH)3电离:H2O+AlO2-+H+?Al(OH)3?Al3++3OH- |
| C、HF溶于水:HF+H2O?H3O++F- |
| D、Na2S溶于水:S2-+2H2O═H2S+2OH- |
下列各组物质中,化学键类型不同的是( )
| A、NaCl和HNO3 |
| B、H2O和NH3 |
| C、CaF2和CsCl |
| D、CCl4和HCl |
下列各组离子在溶液中按括号内的物质的量之比混合,不能得到无色、碱性、澄清溶液的是( )
| A、Na+、Al3+、Cl-、OH-(5:1:4:4) |
| B、NH4+、Ba2+、OH-、Cl-(1:1:1:2) |
| C、Fe3+、Na+、Cl-、S2-(2:1:5:1) |
| D、K+、H+、I-、HCO3-( 2:1:1:2) |