题目内容
12.某有机物A由C、H、O三种元素组成,相对分子质量为90.将9.0克A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4克和13.2克.A能与NaHCO3溶液发生反应,且2分子A之间脱水可生成六元环化合物.关于A的说法正确的是( )| A. | 分子式是C3H8O3 | |
| B. | A催化氧化的产物能发生银镜反应 | |
| C. | 0.1molA与足量Na反应能够产生2.24LH2(标准状况) | |
| D. | A在一定条件下能发生加聚反应 |
分析 由一定质量有机物燃烧产物可计算有机物的实验式,再根据相对分子质量可计算并写出分子式;根据A能与NaHCO3溶液发生反应,可写出A的结构简式;由结构简式即可判断该有机物的性质并计算与钠产生氢气的量,以此解答该题.
解答 解:A.根据分析可知,该有机物的分子式为:C3H6O3,故A错误;
B.由可与NaHCO3溶液发生反应可知A含羧基,再根据2分子A之间脱水可生成六元环化合物,可推出A还含羟基,因此A的结构简式为:CH3-CH(OH)-COOH,A中含羟基,可被催化氧化为醛基或羰基,含醛基的可发生银镜反应,而羰基不能发生银镜反应,故B错误;
C.羟基和羧基均和钠反应,因此0.1molA与足量Na反应产生2.24 L H2(标准状况),故C正确;
D.含有羧基、羟基,不含碳碳双键,则不能发生加聚反应,故D错误.
故选C.
点评 本题考查了有机物分子式的确定,侧重于学生的分析、计算能力的考查,题目难度中等,根据质量守恒判断该有机物分子中含有氧元素的物质的量为解答关键,注意掌握常见有机物结构与性质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.如图是某课外活动小组设计的用化学电池使LED灯发光的装置.下列说法错误的是( )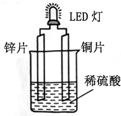

| A. | 铜片表面有气泡生成 | |
| B. | 装置中存在“化学能→电能→光能”的转换 | |
| C. | 如果将铜片换成铁片,电路中的电流方向将改变 | |
| D. | 如果将铜片换成银片,LED灯仍正常发光 |
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1 mol Na与乙醇完全反应,失去2 NA个电子 | |
| B. | 常温常压下,8 g CH4含有5 NA个电子 | |
| C. | 1 L 0.1 mol•L-1的醋酸溶液中含有0.1 NA个H+ | |
| D. | 标准状况下,22.4 L苯含有NA个C6H6分子 |
7.下列有关说法不正确的是( )
| A. | 可以利用丁达尔效应区别胶体和溶液 | |
| B. | 往醋酸溶液中通入足量氨气溶液导电能力变强 | |
| C. | 往FeCl3饱和溶液中逐滴加入浓NaOH溶液边滴加边振荡,可以制得Fe(OH)3胶体 | |
| D. | 丙烯醛(结构简式为CH2═CH-CHO)在一定条件下与H2充分反应生成1-丙醇 |
17.可用于鉴别以下三种化合物的一组试剂是( )
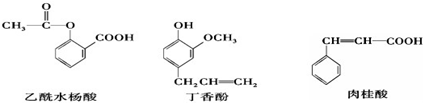
①溴的四氯化碳溶液 ②银氨溶液 ③三氯化铁溶液 ④氢氧化钠溶液.

①溴的四氯化碳溶液 ②银氨溶液 ③三氯化铁溶液 ④氢氧化钠溶液.
| A. | ②④ | B. | ①③ | C. | ③④ | D. | ①② |
1.Q、W、X、Y、Z是原子序数依次增大的短周期主族元素,Q、Y在周期表中相对位置如下:
已知:Q元素最低负化合价的绝对值与其原子最外层电子数相等,W、Y同主族,X是地壳中含量最多的金属元素.下列说法正确的是( )
| Q | ||||
| Y |
| A. | Q的最高价氧化物属于离子化合物 | |
| B. | W和氢元素组成的化合物分子中只含有极性共价键 | |
| C. | Q、X、Y、Z元素最高价氧化物对应的水化物中酸性最强的是HZO4 | |
| D. | 工业上可用电解熔融的X的氯化物方法来制备X单质 |
10.T℃时,在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Z的百分含量与时间的关系如图2所示.则下列结论正确的是( )
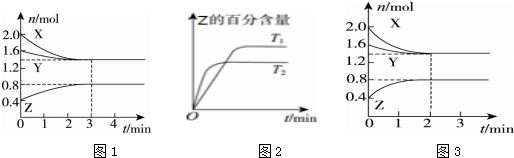

| A. | 容器中发生的反应可表示为3X(g)+Y(g)═2Z(g) | |
| B. | 反应进行的前3 min内,用X表示的反应速率v(X)=0.2 mol/(L•min) | |
| C. | 保持其他条件不变,升高温度,反应的化学平衡常数K减小 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
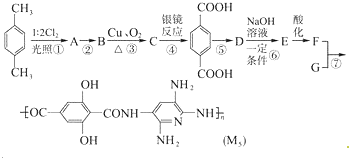
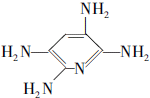 ,F的含氧官能团的名称有羧基、(酚)羟基.
,F的含氧官能团的名称有羧基、(酚)羟基.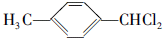 .
.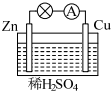 如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )
如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )